Este texto não substitui o publicado no Diário Oficial da União

Gabinete do Ministro
PORTARIA Nº 2.981, DE 26 DE NOVEMBRO DE 2009(*)
(Revogada pela PRT nº 1554/GM/MS de 30.07.2013)
(Republicada pelo DOU Nº 229 de 01.12.2009, seção 1, pág 71)
Aprova o Componente Especializado da Assistência Farmacêutica.
O MINISTRO DE ESTADO DA SAÚDE, no uso das atribuições que lhe conferem os incisos I e II do parágrafo único do art. 87 da Constituição, e
Considerando as diretrizes estabelecidas pela Política Nacional de Medicamentos, constante da Portaria nº 3.916/GM, de 30 de novembro de 1998;
Considerando os princípios e eixos estratégicos definidos pela Política Nacional de Assistência Farmacêutica aprovada pela Resolução nº 338, de 2004, do Conselho Nacional de Saúde;
Considerando as Portarias nº 399/GM, de 22 de fevereiro de 2006, que Divulga o Pacto pela Saúde e nº 204/GM, de 29 de janeiro de 2007, que regulamenta o financiamento e a transferência dos recursos federais na forma de blocos de financiamento;
Considerando a necessidade de aprimorar os instrumentos e estratégias que asseguram e ampliam o acesso da população aos serviços de saúde, incluído o acesso aos medicamentos em estreitarelação com os princípios da Constituição e da organização do Sistema Único de Saúde; e
Considerando a pactuação na reunião da Comissão Intergestores Tripartite de 24 de setembro de 2009, resolve:
Art. 1º Regulamentar e aprovar, no âmbito do Sistema Único de Saúde, o Componente Especializado da Assistência Farmacêutica como parte da Política Nacional de Assistência Farmacêutica, integrante do Bloco de Financiamento da Assistência Farmacêutica, conforme definido no Capítulo I desta Portaria.
Art. 2º Alterar a denominação do Componente de Medicamentos de Dispensação Excepcional descrito no inciso III, art. 24º, seção IV, da Portaria nº 204/GM, de 29 de janeiro de 2007, para Componente Especializado da Assistência Farmacêutica.
Art. 3º Alterar a denominação do Subgrupo 01 - Medicamentos de Dispensação Excepcional doGrupo 06 - Medicamentos da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e MateriaisEspeciais do Sistema Único de Saúde, para Componente Especializado da Assistência Farmacêutica, que deverá ser utilizado pelos gestores para fins de cadastro da Produção Ambulatorial.
Art 4º Alterar a denominação da classificação 001 - Dispensação de Medicamentos Excepcionais/ Especiais do Código de Serviço 125 - Serviço de Farmácia da Tabela de Serviços/Classificações do Sistema de Cadastro Nacional de Estabelecimentos de Saúde (SCNES), descrito no Anexo I da Portaria nº 154/SAS, de 18 de março de 2008, para Dispensação de Medicamentos do Componente Especializado da Assistência Farmacêutica.
Art 5º Cabe ao Departamento de Regulação, Avaliação e Controle de Sistemas (DRAC), da Secretaria de Atenção à Saúde (SAS) do Ministério da Saúde, providenciar, junto ao Departamento de Informática do SUS (DATASUS/SE/MS), as medidas necessárias para que sejam efetivadas nos Sistemas de Informações, as adequações definidas nesta Portaria.
Art. 6º Caberá à Secretaria de Ciência, Tecnologia e Insumos Estratégicos do Ministério da Saúde editar normas complementares referentes à operacionalização do Componente Especializado da Assistência Farmacêutica, observadas as pactuações na Comissão Intergestores Tripartite (CIT).
Art. 7º Definir que os recursos orçamentários de que trata esta Portaria corram por conta da funcional programática 10303.1293.4705.0001 do orçamento do Ministério da Saúde.
CAPÍTULO I - DA DEFINIÇÃO
Art. 8º O Componente Especializado da Assistência Farmacêutica é uma estratégia de acesso amedicamentos no âmbito do Sistema Único de Saúde, caracterizado pela busca da garantia da integralidade do tratamento medicamentoso, em nível ambulatorial, cujas linhas de cuidado estão definidas em Protocolos Clínicos e Diretrizes Terapêuticas publicados pelo Ministério da Saúde.
Parágrafo único. O acesso aos medicamentos que fazem parte das linhas de cuidado para as doenças contempladas no âmbito deste Componente será garantido mediante a pactuação entre a União, estados, Distrito Federal e municípios, conforme as diferentes responsabilidades definidas nesta Portaria.
CAPÍTULO II - DA ORGANIZAÇÃO
Art. 9º Os medicamentos que fazem parte das linhas de cuidado para as doenças contempladas neste Componente estão divididos em três grupos com características, responsabilidades e formas de organização distintas.
Grupo 1 - Medicamentos sob responsabilidade da União
Grupo 2 - Medicamentos sob responsabilidade dos Estados e Distrito Federal
Grupo 3 - Medicamentos sob responsabilidade dos Municípios e Distrito Federal
Art. 10. Os grupos foram constituídos considerando os seguintes critérios gerais:
I - complexidade da doença a ser tratada ambulatorialmente;
II - garantia da integralidade do tratamento da doença no âmbito da linha de cuidado;
III - manutenção do equilíbrio financeiro entre as esferas de gestão.
Art. 11. O Grupo 1 foi constituído sob os seguintes critérios:
I - maior complexidade da doença a ser tratada ambulatorialmente;
II - refratariedade ou intolerância a primeira e/ou a segunda linha de tratamento;
III - medicamentos que representam elevado impacto financeiro para o Componente;
IV - medicamentos incluídos em ações de desenvolvimento produtivo no complexo industrial da saúde.
Art. 12. O Grupo 2 foi constituído sob os seguintes critérios:
I - menor complexidade da doença a ser tratada ambulatorialmente em relação aos elencados no Grupo 1;
II - refratariedade ou intolerância a primeira linha de tratamento.
Art. 13. O Grupo 3 foi constituído sob os seguintes critérios:
I - fármacos constantes na Relação Nacional de Medicamentos Essenciais vigente e indicados pelos Protocolos Clínicos e Diretrizes Terapêuticas, publicados na versão final pelo Ministério da Saúde, como a primeira linha de cuidado para o tratamento das doenças contempladas neste Componente.
Art. 14. O elenco de medicamentos em cada grupo está descrito nos Anexos I, II e III desta Portaria.
Parágrafo único. Os medicamentos deste Componente deverão ser autorizados somente para as doenças (descritas de acordo com o CID-10) constantes no Anexo IV a esta Portaria.
Art. 15. Os medicamentos dos Grupos 1 e 2 sob responsabilidade da União, Estados e DistritoFederal compõem o Grupo 06, Subgrupo 01 da Tabela de Procedimentos, Medicamentos, Órteses,Próteses e Materiais Especiais do Sistema Único de Saúde, na forma e redação estabelecidas no Anexo IV a esta Portaria.
§ 1º Os atributos idade mínima, idade máxima, sexo, quantidade máxima e CID-10 da Tabelade Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde foram estabelecidos de acordo com os critérios estabelecidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
§ 2º O atributo quantidade máxima foi definido considerando os meses com 31 dias. Para os meses com até 30 dias, a quantidade máxima autorizada será diretamente proporcional a quantidade de dias do mês correspondente.
Art. 16. As formas de organização dos procedimentos do Grupo 06, Subgrupo 01, da Tabela deProcedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde foram redefinidas segundo os critérios de classificação da Anatomical Therapeutic Chemical (ATC) da Organização Mundial da Saúde.
§ 1º Fármacos da mesma forma de organização não deverão ser autorizados para uma mesma doença no mesmo período de vigência da APAC (Autorização de Procedimentos Ambulatoriais), exceto nos casos de recomendação dos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
§ 2º Fármacos da mesma forma de organização poderão ser autorizados para doenças diferentes no mesmo período de vigência da APAC, exceto para a forma de organização dos inibidores do fator de necrose tumoral alfa.
Art. 17. Cabe a esfera de gestão responsável, a seleção dos medicamentos entre as formas deorganização da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais doSistema Único de Saúde que define os procedimentos dos Grupos 1 e 2, desde que garantidas as linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde.
Parágrafo único. A não disponibilização de medicamentos no âmbito deste Componente não garante a integralidade do tratamento, provocando desequilíbrio financeiro, devendo os gestores do SUS, em pactuação na CIT, promover ações que restabeleçam a garantia do acesso aos medicamentos estabelecidos nas linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde e o equilíbrio financeiro.
Art. 18. A incorporação, exclusão ou substituição de medicamentos ou ampliação de cobertura para medicamentos já padronizados no âmbito deste Componente, ocorrerá mediante os critérios estabelecidos pela Comissão de Incorporação de Tecnologias do Ministério da Saúde (CITEC/MS), con-forme ato normativo específico e pactuação na CIT.
§ 1º O impacto orçamentário das incorporações ou ampliação de cobertura para medicamentos já incorporados será calculado pelo Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde, visando auxiliar o processo de tomada de decisão a partir da análise da incorporação pela CITEC/MS e a pactuação no âmbito da CIT.
§ 2º A responsabilidade pelo financiamento das incorporações (de novos medicamentos, de ampliação de cobertura para medicamentos já incorporados e incorporações de novas concentrações e/ou apresentações farmacêuticas) deverá ser pactuada no âmbito da CIT, respeitando-se a manutenção do equilíbrio financeiro entre as esferas de gestão e a garantia da linha de cuidado da doença.
Art. 19. A incorporação efetiva de um medicamento nos Grupos 1, 2 e 3 deste Componente ocorrerá somente após a publicação na versão final do Protocolo Clínico e Diretrizes Terapêuticas específico pelo Ministério da Saúde, observadas as pactuações na CIT.
Art. 20. O Ministério da Saúde, em pactuação na CIT, poderá avaliar a transferência, em qualquer momento, de medicamentos deste Componente para outros Componentes do Bloco da Assistência Farmacêutica ou a transferência entre os Grupos 1, 2 e 3, garantindo a disponibilização desses medicamentos no âmbito do SUS e o equilíbrio financeiro entre as esferas de gestão.
Art. 21. Para os medicamentos excluídos por esta Portaria, transferidos para outros Componentes ou que posteriormente possam ser excluídos do elenco deste Componente por meio de Portarias específicas, será considerado o prazo de 120 dias a partir da publicação da respectiva Portaria, paraapresentação das APAC no Sistema de Informações Ambulatoriais do Sistema Único de Saúde (SIA/SUS), geradas a partir da dispensação.
Art. 22. Os medicamentos do Grupo 3 são de responsabilidade dos Municípios e do Distrito Federal e compõem parte do Elenco de Referência Nacional do Componente Básico da Assistência Farmacêutica regulamentado por ato normativo específico, devendo ser disponibilizados para a garantia das linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
Art. 23. Foram excluídos os seguintes procedimentos do Grupo 06, Subgrupo 01 da Tabela de
Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde:

Art. 24. Os medicamentos do Grupo 06, Subgrupo 01, da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde relacionados abaixo foram transferidos para o Componente Básico da Assistência Farmacêutica, considerando o art. 9º desta Portaria:

CAPÍTULO III - DA EXECUÇÃO
Art. 25. A execução do Componente envolve as etapas de solicitação, avaliação, autorização,
dispensação dos medicamentos e renovação da continuidade do tratamento.
Parágrafo único. Os medicamentos do Grupo 3 são regulamentados no âmbito do Componente Básico da Assistência Farmacêutica em ato normativo específico.
Art. 26. Para os medicamentos constantes dos Grupos 1 e 2, a execução é descentralizada às Secretarias Estaduais de Saúde, devendo ser realizada de acordo com os critérios definidos nesta Portaria.
Art. 27. A solicitação, dispensação e renovação da continuidade do tratamento deverão ocorrer somente em estabelecimentos de saúde vinculados às unidades públicas designados pelos gestores estaduais.
Art. 28. A solicitação, dispensação e a renovação da continuidade do tratamento poderão ser descentralizadas junto à rede de serviços públicos dos municípios mediante pactuação entre os gestores estaduais e municipais, desde que respeitado o disposto no art. 26 desta Portaria, os critérios legais e sanitários vigentes e os demais critérios de execução deste Componente.
Art. 29. As Secretarias Estaduais de Saúde deverão manter os Municípios informados sobre a sistemática de execução deste Componente e os critérios de acesso aos medicamentos dos Grupos 1 e 2.
A - Da solicitação
Art. 30. A solicitação de medicamentos corresponde ao pleito do paciente ou seu responsável na unidade designada pelo gestor estadual conforme art. 27 desta Portaria. Para a solicitação dos medicamentos serão obrigatórios os seguintes documentos do paciente:
I - cópia do Cartão Nacional de Saúde (CNS);
II - cópia de documento de identidade - caberá ao responsável pelo recebimento da solicitação atestar a autenticidade de acordo com o documento original;
III -Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido;
IV - prescrição médica devidamente preenchida;
V - documentos exigidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado; e
VI - cópia do comprovante de residência.
Art. 31. No processo de solicitação, o paciente poderá designar representante(s) para a retirada do medicamento. Para o cadastro de representante(s) serão exigidos os seguintes documentos, que deverão ser apresentados e inseridos junto com os documentos para a solicitação: declaração autorizadora, nome e endereço completos, cópia do documento de identidade e número de telefone da pessoa autorizada.
Parágrafo único. Fica dispensada a presença dos pacientes aqueles considerados incapazes, conforme arts. 3º e 4º do Código Civil, e devidamente caracterizados no LME, pelo médico prescritor.
Art. 32. Cada usuário deverá ter apenas um único cadastro no Componente, independente do número de LME vigentes.
B - Da avaliação
Art. 33. O avaliador deverá ser um profissional de saúde com ensino superior completo, registrado em seu devido conselho de classe e designado pelo gestor estadual.
Art. 34. Para a avaliação técnica da solicitação dos medicamentos, deverão ser considerados os documentos exigidos no art. 30, observando-se:
I - Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido, de acordo com as instruções apresentadas no Anexo V a esta Portaria;
II - prescrição médica contendo as informações exigidas na legislação vigente; e
III - todos os documentos exigidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado.
Parágrafo único. A análise técnica da solicitação deve ser realizada considerando os campos referentes à avaliação descrita no LME, conforme as instruções apresentadas no Anexo V a esta Portaria.
C - Da autorização
Art. 35. O autorizador deverá ser um profissional de nível superior completo, preferencialmente da área da saúde, designado pelo gestor estadual.
Art. 36. A autorização do LME deverá ser efetivada somente após o deferimento da avaliação realizada de acordo com o art. 33 e art. 34 desta Portaria.
D - Da dispensação
Art. 37. A dispensação do medicamento deverá ser efetivada somente após a autorização realizada de acordo com o art. 35 e art. 36 desta Portaria.
Art. 38. No ato da dispensação, o recibo de dispensação do medicamento deverá estar devidamente preenchido e assinado.
Parágrafo único. O Recibo de Medicamentos (RME) a ser utilizado no âmbito deste Componente deverá conter, no mínimo, os dados constantes no modelo apresentado no Anexo VI a esta Portaria.
Art. 39. Uma via do LME, os recibos de dispensação dos medicamentos e os documentos descritos no art. 30 desta Portaria deverão ser mantidos em arquivo pelo prazo estabelecido na legislação em vigor.
Art. 40. A dispensação do medicamento poderá ser realizada para mais de um mês de competência, dentro do limite de vigência da APAC e respeitadas as exigências legais.
Art. 41. O processamento mensal da APAC no Sistema SIA/SUS deverá ser efetivado somente a partir da emissão do recibo de dispensação do medicamento contendo a assinatura do usuário ou seu representante.
Art. 42. A interrupção do fornecimento por abandono do tratamento deverá ser realizada quando
o paciente ou representante não retirar o medicamento por três meses consecutivos e não tiver ocorrido
o fornecimento antecipado, previsto no art. 40 desta Portaria.
Art. 43. O Sistema SIA/SUS exercerá crítica para todos os medicamentos dos Grupos 1 e 2 doComponente, conforme os atributos da Tabela de Procedimentos, Medicamentos, Órteses, Próteses eMateriais Especiais do Sistema Único de Saúde, apresentada no Anexo IV a esta Portaria.
E - Da renovação
Art. 44. Para a renovação da continuidade do tratamento serão obrigatórios os seguintes documentos do paciente:
I - Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido, de acordo com as instruções apresentadas no Anexo V desta Portaria;
II - prescrição médica contendo as informações exigidas na legislação vigente; e
III - todos os documentos para monitoramento do tratamento estabelecidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado.
CAPÍTULO IV
DA PROGRAMAÇÃO, AQUISIÇÃO, ARMAZENAMENTO E DISTRIBUIÇÃO
Art. 45. A responsabilidade pela programação, armazenamento e distribuição dos medicamentos
dos Grupos 1A e 1B do Anexo I a esta Portaria é das Secretarias Estaduais de Saúde, sendo a
responsabilidade pela aquisição dos medicamentos do Grupo 1A do Ministério da Saúde e dos medicamentos
do Grupo 1B das Secretarias Estaduais de Saúde.
Art. 46. A responsabilidade pela programação, aquisição, armazenamento e distribuição dos medicamentos do Grupo 2 do Anexo II desta Portaria é de responsabilidade das Secretarias Estaduais de Saúde.
Art. 47. A responsabilidade pela programação, aquisição, armazenamento e distribuição dos medicamentos do Grupo 3 é dos Municípios e está estabelecida em ato normativo específico que regulamenta o Componente Básico da Assistência Farmacêutica.
Art. 48. Na aquisição dos medicamentos dos Grupos 1 e 2, os gestores deverão observar o Preço Máximo de Venda ao Governo (PMVG) conforme regulamentação vigente da Câmara de Regulação do Mercado de Medicamentos (CMED) e os preços praticados no mercado, no sentido de obter a proposta mais vantajosa para a administração pública.
Parágrafo único. Os responsáveis pelas aquisições deverão verificar, ainda, a aplicação dos benefícios fiscais que incidem sobre os medicamentos listados nos Convênios ICMS (CONFAZ) vi-gentes.
CAPÍTULO V
DOS MEDICAMENTOS DE AQUISIÇÃO CENTRALIZADA PELO MINISTÉRIO DA SAÚ-DE
Art. 49. O Ministério da Saúde, as Secretarias Estaduais de Saúde e o Distrito Federal poderão pactuar a aquisição centralizada dos medicamentos pertencentes ao Grupos 1B (conforme o Anexo I) e Grupo 2 (conforme Anexo II) deste Componente, desde que seja garantido o equilíbrio financeiro entre as esferas de gestão, observando, entre outros, o benefício econômico da centralização frente às condições do mercado e os investimentos estratégicos do governo no desenvolvimento tecnológico e da capacidade produtiva junto aos laboratórios públicos e oficiais.
Art. 50. Os medicamentos a seguir identificados serão adquiridos por meio de processo centralizado
no Ministério da Saúde.

§ 1º A distribuição dos medicamentos cuja aquisição é de responsabilidade do Ministério da Saúde ocorrerá a partir da finalização dos procedimentos administrativos indispensáveis para o processo de aquisição.
§ 2º O valor desses medicamentos na Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde corresponderá a zero a partir da primeira distribuição realizada pelo Ministério da Saúde.
§ 3º Após a primeira distribuição dos medicamentos de aquisição centralizada, o Ministério da Saúde realizará o ressarcimento correspondente ao estoque estadual com base nas APAC faturadas no prazo de 180 dias, considerando os valores definidos anteriormente ao zeramento da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
Art. 51. A dispensação dos medicamentos de aquisição centralizada pelo Ministério da Saúde é de responsabilidade das Secretarias Estaduais de Saúde e deve seguir os critérios estabelecidos no Capítulo III desta Portaria.
A - Da programação anual
Art. 52. As Secretarias Estaduais de Saúde deverão encaminhar ao Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde a programação anual de cada medicamento de aquisição centralizada.
Parágrafo único. A programação anual dos medicamentos é de responsabilidade das Secretarias Estaduais de Saúde e deverá ser enviada no período de 1º a 20 de julho de cada ano, devendo considerar a média das APAC aprovadas nos seis (6) meses anteriores. Mediante apresentação de justificativa e avaliação do Ministério da Saúde, será permitido incremento de até 20% para o período.
B - Da programação trimestral
Art. 53. As Secretarias Estaduais de Saúde deverão encaminhar ao Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde a necessidade trimestral de cada medicamento de aquisição centralizada, conforme cronograma abaixo:
§ 1º O quantitativo a ser distribuído para o trimestre deverá considerar também a programação anual.
§ 2º A distribuição dos medicamentos seguirá o período de entrega estabelecido no cronograma abaixo:
C - Do controle e monitoramento da programação
Art. 54. A distribuição dos medicamentos adquiridos de forma centralizada pelo Ministério da Saúde terá como parâmetros a programação anual enviada pelas Secretarias Estaduais de Saúde e a continuidade e regularidade da produção registrada em APAC.
Art. 55. Após a finalização da programação anual pelas Secretarias Estaduais de Saúde para os medicamentos de aquisição centralizada pelo Ministério da Saúde, caso seja verificado que o consumo, via produção registrada em APAC, para o período anual seja inferior ao quantitativo total distribuído, a diferença será ajustada na programação seguinte.
Art. 56. Após a entrega dos medicamentos de aquisição centralizada pelo Ministério da Saúde, toda logística restante será de responsabilidade exclusiva dos Estados e do Distrito Federal.
CAPÍTULO VI - DO FINANCIAMENTO
Art. 57. O financiamento para aquisição dos medicamentos do Componente estará diretamente relacionado ao grupo em que os estes estão alocados.
Art. 58. Os medicamentos do Grupo 3 serão financiados de acordo com a regulamentação do Componente Básico da Assistência Farmacêutica, em ato normativo específico.
Art. 59. Os medicamentos pertencentes ao Grupo 2 serão financiados integralmente pelos Estados e Distrito Federal, observando o disposto no art. 48 deste Componente.
Parágrafo único. A Tabela de Procedimentos, Medicamentos, Órteses, Próteses e MateriaisEspeciais do Sistema Único de Saúde para os medicamentos do Grupo 2 terá o valor igual a zero a partir da vigência desta Portaria.
Art. 60. Os medicamentos pertencentes ao Grupo 1 serão financiados pelo Ministério da Saúde na forma de aquisição centralizada (Grupo 1A), conforme definições do Capítulo V desta Portaria, e na forma de transferência de recursos financeiros (Grupo 1B).
Art. 61. Os valores dos medicamentos financiados pelo Ministério da Saúde e adquiridos pelasSecretarias Estaduais da Saúde da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde serão calculados considerando o PMVG conforme regulamentação vigente da CMED, observando o disposto no art. 48 e terão validade a partir da vigência desta Portaria.
§ 1º Para os medicamentos que não estão sujeitos ao Coeficiente de Adequação de Preço (CAP), o PMVG será considerado como o Preço de Fábrica definido pela CMED.
§ 2º Caso o valor praticado no mercado seja inferior ao estabelecido pelo PMVG, o financiamento será calculado com base na média ponderada dos valores praticados, definidos pelos valores atualizados do Banco de Preços em Saúde ou por meio da solicitação de preço aos Estados e ao Distrito Federal.
Art. 62. Os valores dos medicamentos constantes da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde serão atualizados anualmente conforme definições de preço da CMED e preços praticados pelos Estados e ao Distrito Federal.
Parágrafo único. A periodicidade da revisão dos valores poderá ser inferior a 12 meses con-forme interesse da administração pública, observando-se a pactuação na CIT.
Art. 63. Trimestralmente, o Ministério da Saúde publicará Portaria com os valores a serem transferidos mensalmente às Secretarias Estaduais de Saúde, apurados com base na média das APAC emitidas e aprovadas conforme critérios e valores de referência indicados para o Grupo 06, Subgrupo 01da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
§ 1º O Ministério da Saúde, por meio do Departamento de Assistência Farmacêutica e Insumos Estratégicos, consolidará as informações no Sistema SIA/SUS até o último dia útil do mês subsequente a apuração da média do trimestre anterior, para publicação de Portaria com os valores a serem transferidos aos Estados.
§ 2º O Fundo Nacional de Saúde repassará aos Fundos Estaduais de Saúde, mensalmente até o décimo quinto dia e na modalidade fundo a fundo, os valores apurados e publicados, os quais deverão ser movimentados em conta específica.
Art. 64. Os recursos do Ministério da Saúde aplicados no financiamento do Grupo 1B terão
como base a emissão e a aprovação das APAC emitidas pelas Secretarias Estaduais de Saúde, vinculadas à efetiva dispensação do medicamento e de acordo com os critérios técnicos definidos nesta Portaria.
CAPÍTULO VII - DO CONTROLE E MONITORAMENTO
Art. 65. A União, os Estados, o Distrito Federal e os Municípios deverão monitorar os recursos aplicados no financiamento do Componente, com vistas a ajustes que assegurem o equilíbrio da responsabilidade e a participação no financiamento entre as esferas de gestão, cujas análises devem ser sustentadas por informações sobre os preços praticados, quantidades adquiridas e número de pacientes atendidos.
Art. 66. As Secretarias Estaduais de Saúde deverão enviar mensalmente ao DATASUS, da Secretaria-Executiva do Ministério da Saúde, as informações, via APAC, dos procedimentos constantes nos Grupos 1 e 2 e selecionados pelas Secretarias Estaduais de Saúde de acordo com o art. 17 desta Portaria, observando o cronograma estabelecido pelo Ministério da Saúde em ato normativo específico.
Parágrafo único. A não emissão das APAC para os medicamentos que compõem o Grupo 2 será entendida como a não garantia da linha de cuidado sob responsabilidade do gestor estadual, podendo acarretar em novas definições no financiamento, no sentido de manter o equilíbrio financeiro entre as esferas de gestão.
Art. 67. De acordo com o art. 6º do Decreto nº 1.651, de 1995, a comprovação da aplicação dos recursos transferidos do Fundo Nacional de Saúde para os Fundos Estaduais de Saúde, na forma do Decreto nº 1.232, de 1994, que trata das transferências fundo a fundo, deverá ser apresentada ao Ministério da Saúde e as Secretarias Estaduais de Saúde, por meio de Relatório de Gestão, aprovado pelo respectivo Conselho de Saúde.
Art. 68. O Ministério da Saúde, juntamente com Estados e Municípios, deverá realizar controle, avaliação e monitoramento sistemático da organização, execução e financiamento, com vistas ao aprimoramento permanente do Componente e a garantia das linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
Parágrafo único. As Secretarias Estaduais de Saúde deverão fornecer ao Ministério da Saúde, sempre que solicitado, informações referentes à organização, a execução, ao acompanhamento e monitoramento do Componente.
Art. 69. Para o controle e monitoramento, o Ministério da Saúde disponibilizará sistema informatizado de gerenciamento e acompanhamento dos medicamentos do Componente.
§ 1º. As Secretarias Estaduais de Saúde deverão adotar o sistema disponibilizado ou outro similar próprio que contemple os requisitos e informações previstos nesta Portaria.
§ 2º O Ministério da Saúde publicará ato normativo para regulamentar e definir as regras de utilização do referido sistema.
CAPÍTULO VIII
DO LAUDO PARA SOLICITAÇÃO, AVALIAÇÃO E AUTORIZAÇÃO DE MEDICAMENTOS DO COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA
Art. 70. O Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME) é o instrumento que deve ser utilizado para execução deste Componente.
Art. 71. O modelo do LME que deverá ser utilizado no âmbito deste Componente e as instruções para o adequado preenchimento estão descritos no Anexo V a esta Portaria.
§ 1º O LME estará estruturado para que seja preenchido com informações sobre a solicitação, avaliação e autorização do procedimento.
§ 2º O preenchimento da solicitação deverá ser realizado pelo médico solicitante. Os campos relativos aos dados complementares do paciente poderão ser preenchidos por outro profissional, desde que cadastrado no mesmo estabelecimento de saúde do médico solicitante.
Art. 72. Para cada doença, definida de acordo com a Classificação Estatística Internacional de doenças e Problemas Relacionados à Saúde (CID-10), haverá a necessidade de preenchimento de um LME.
§ 1º Cada LME corresponderá a uma única APAC.
§ 2º Em caso de solicitação de mais de cinco medicamentos para a mesma doença (CID-10), o mesmo médico deverá preencher mais de um LME. Nesse caso, deverá ser emitido apenas um número de APAC.
§ 3º Durante o período de vigência da APAC de um LME será permitido o ajuste da solicitação da seguinte forma: substituição, inclusão ou exclusão de procedimentos para o tratamento da mesma doença (CID-10) ou alteração da quantidade solicitada pelo médico, caracterizando adequação do LME.
§ 4º Nos casos em que o medicamento não tiver indicação para utilização contínua, deverá ser emitida APAC única, que corresponderá apenas ao mês de atendimento
Art. 73. Será permitida a emissão de mais de uma APAC dentro do mesmo período de vigência, nos casos de pacientes diagnosticados com mais de uma doença (CID-10).
Art. 74. O LME terá sessenta (60) dias de validade para solicitação do medicamento, a partir de sua data de preenchimento pelo médico solicitante.
Art. 75. Para cada LME deverá ser emitido um parecer do avaliador.
Parágrafo único. Caso seja solicitado mais de um medicamento no mesmo LME, a avaliação poderá possuir mais de um parecer.
Art. 76. O LME será assinado somente pelo autorizador nos casos de deferimento de um medicamento pelo avaliador.
Art. 77. Esta Portaria entrará em vigor após noventa (90) dias da sua publicação.
Art. 78. Ficam revogadas as Portarias nº 1.259/GM, de 17 de junho de 2009, publicada no Diário Oficial da União nº 114, de 18 junho de 2009, Seção I, página 44; nº 106/GM, de 22 de janeiro de 2009, publicada no Diário Oficial nº 16, de 23 de janeiro de 2009, Seção I, página 40; nº 850/GM, de 20 de abril de 2007, publicada no Diário Oficial da União nº 77, de 23 de abril de 2007, Seção I, página 26; Portarias nº 1.320/GM, de 5 de junho de 2007, publicada no Diário Oficial da União nº 108, de 6 junho de 2007, Seção I, página 65; nº 2.577/GM, de 27 de outubro de 2006, publicada no Diário Oficial da União nº 208, de 30 outubro de 2006, Seção I, página 147; nº 3.227/GM, de 20 de dezembro de 2006, publicada no Diário Oficial da União nº 244, de 21 de dezembro de 2006, Seção I, página 76 nº 1.654/GM, de 11 de agosto de 2004, publicada no Diário Oficial da União nº 162, de 12 de agosto de 2004, Seção I, página 53; nº 971/GM, de 3 de julho de 2001, publicada no Diário Oficial da União nº 128, de 4 de julho de 2001, Seção I, página 121; nº 254/GM, de 31 de março de 1999, publicada no Diário Oficial da União nº 62, de 1º de abril de 1999, Seção I, página 10; nº 14/SCTIE, de 19 de dezembro de 2008, publicada no Diário Oficial da União nº 248, de 22 de dezembro de 2008, Seção I, página 289; nº 341/SAS, de 22 de agosto de 2001, publicada no Diário Oficial da União nº 162, de 23 de agosto de 2001, Seção I, página 50; nº 14/SAS, de 14 de janeiro de 1999, publicada no Diário Oficial da União nº 162, de 15 de janeiro de 1999, Seção I, página 10; nº 105/SAS, de 29 de março de 1999, publicada no Diário Oficial da União nº 60 de 30 de março de 1999, Seção I, página 44; nº 138/SAS, de 20 de abril de 1999, publicada no Diário Oficial da União nº 76, de 23 de abril de 1999, Seção I, página 112; nº 50/SAS, de 21 de junho de 1995, publicada no Diário Oficial da União nº 118, de 22 de junho de 1995, Seção I, página 9168; nº 112/SAS, de 6 de outubro de 1993, publicada no Diário Oficial da União nº 198, de 18 de outubro de 1993, Seção I, página 15541; e o Anexo II da Portaria nº 768/SAS, de 26 de outubro de 2006, publicada no Diário Oficial da União nº 207, de 27 de outubro de 2006, Seção I, página 91.
JOSÉ GOMES TEMPORÃO
ANEXO I
GRUPO 1A: Medicamentos com aquisição centralizada pelo Ministério da Saúde para tratamento das doenças contempladas neste Componente.

GRUPO 1B: Medicamentos financiados com transferência de recursos financeiros pelo Ministério da
Saúde para tratamento das doenças contempladas neste Componente.

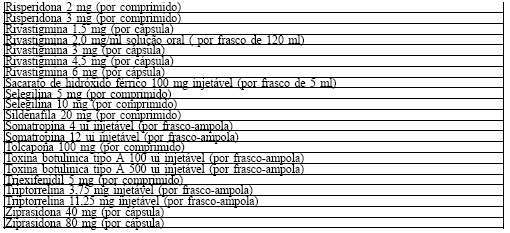
ANEXO II
GRUPO 2: Medicamentos financiados pelas Secretarias de Estado da Saúde para tratamento das doenças
contempladas neste Componente.


ANEXO III
GRUPO 3: Medicamentos cuja dispensação é de responsabilidade dos municípios e Distrito Federal para
tratamento das doenças contempladas neste Componente.

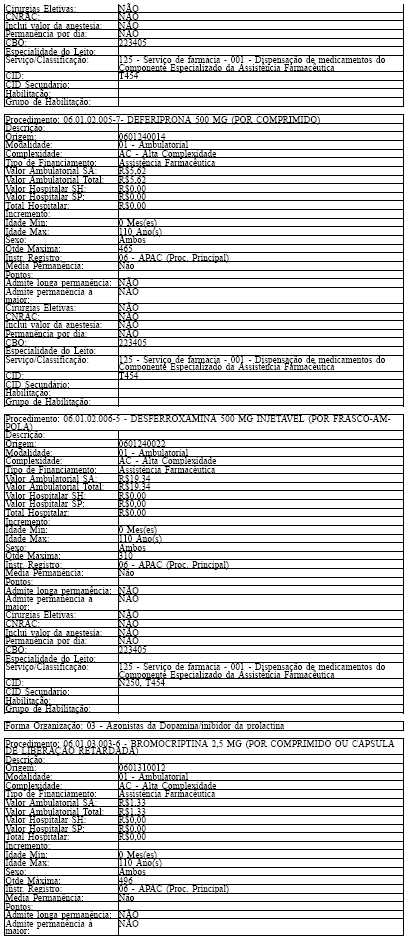
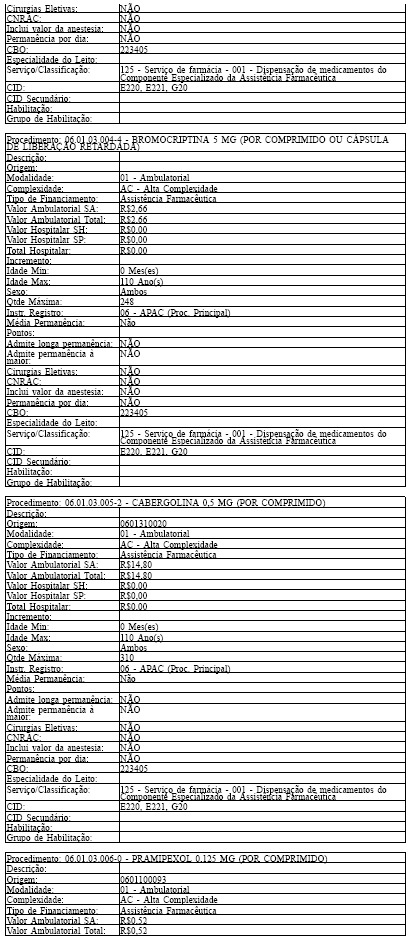
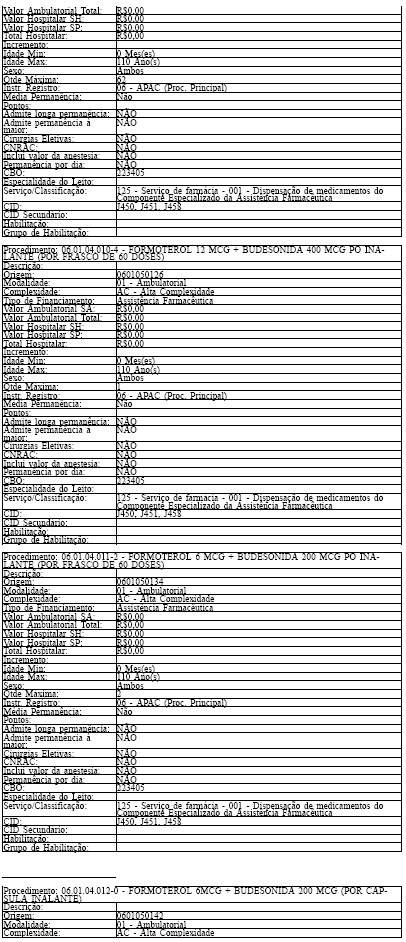
ANEXO IV
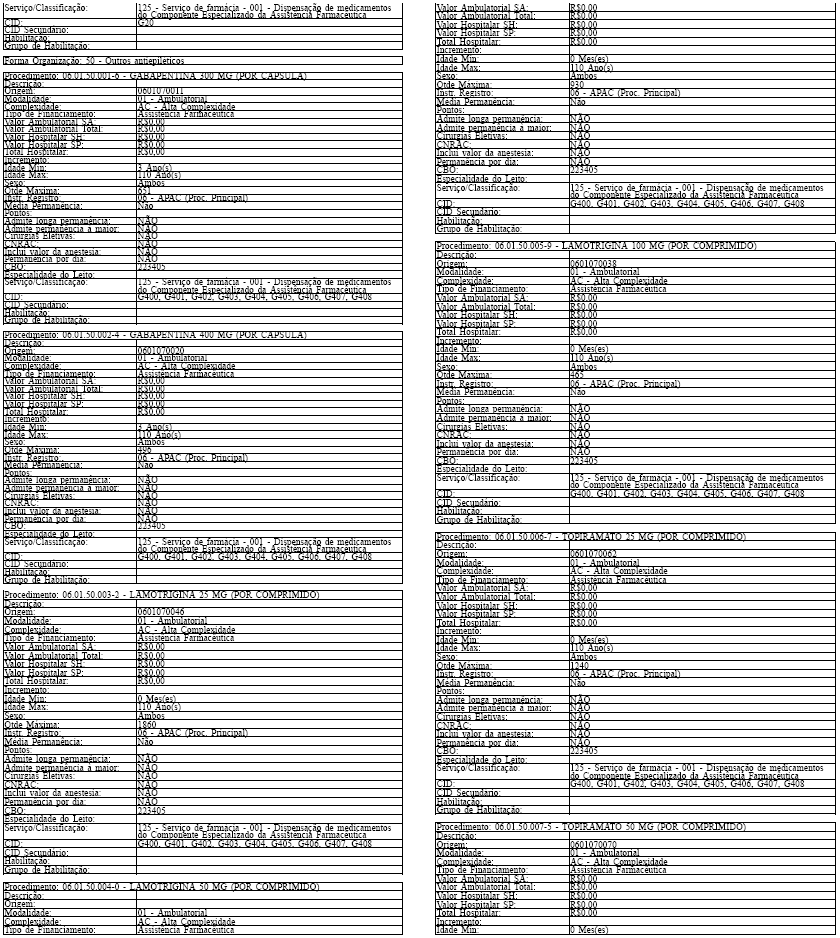
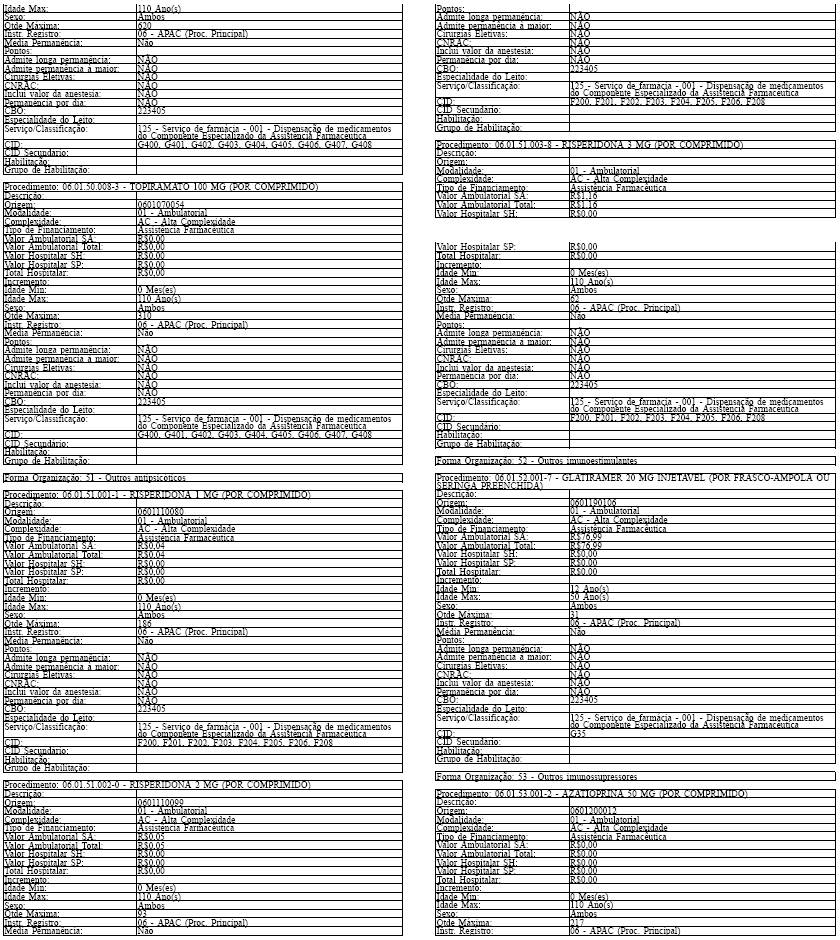
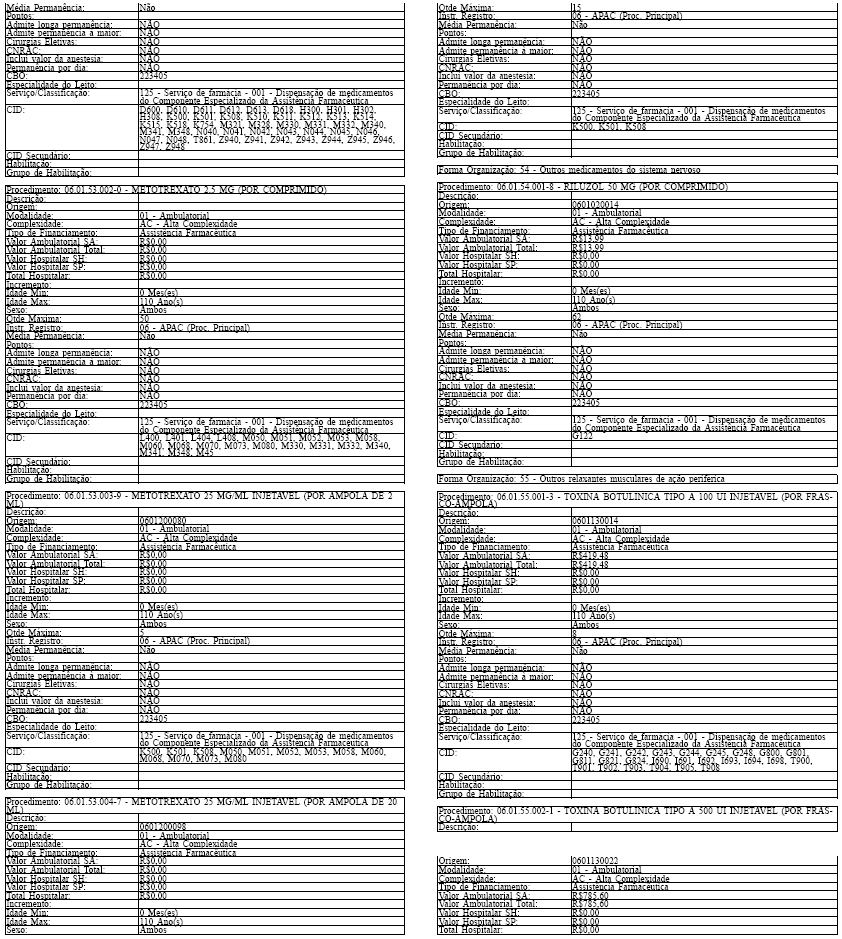
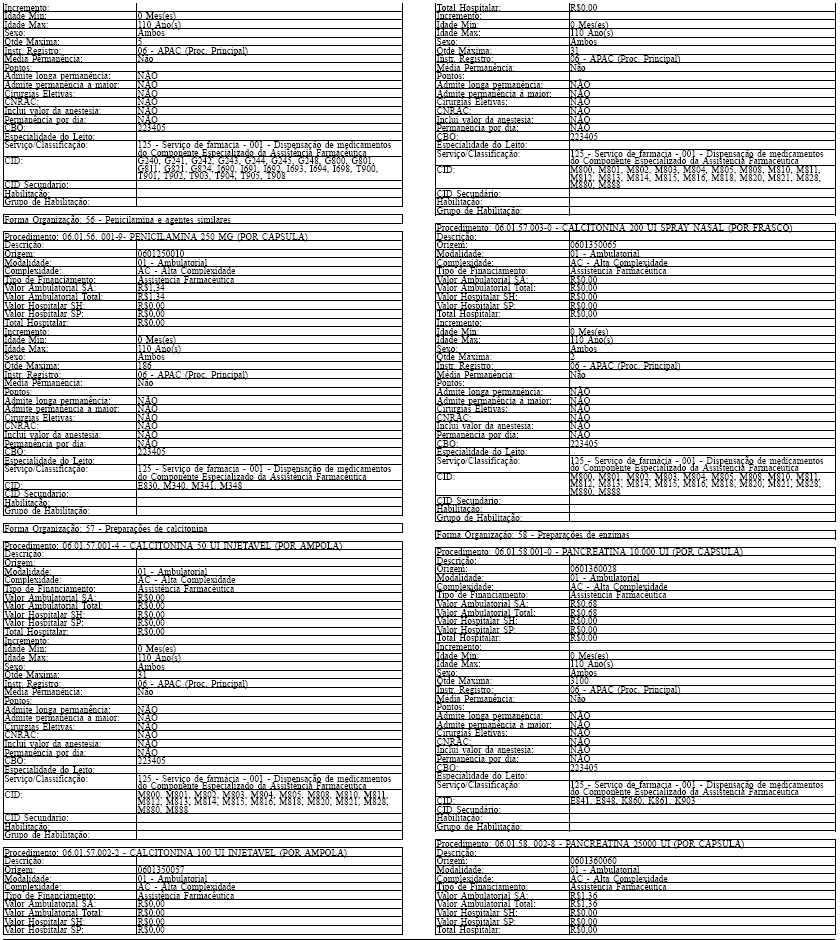
Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único
de Saúde
Grupo: 06 - Medicamentos
Sub Grupo: 01 - Componente Especializado da Assistência Farmacêutica























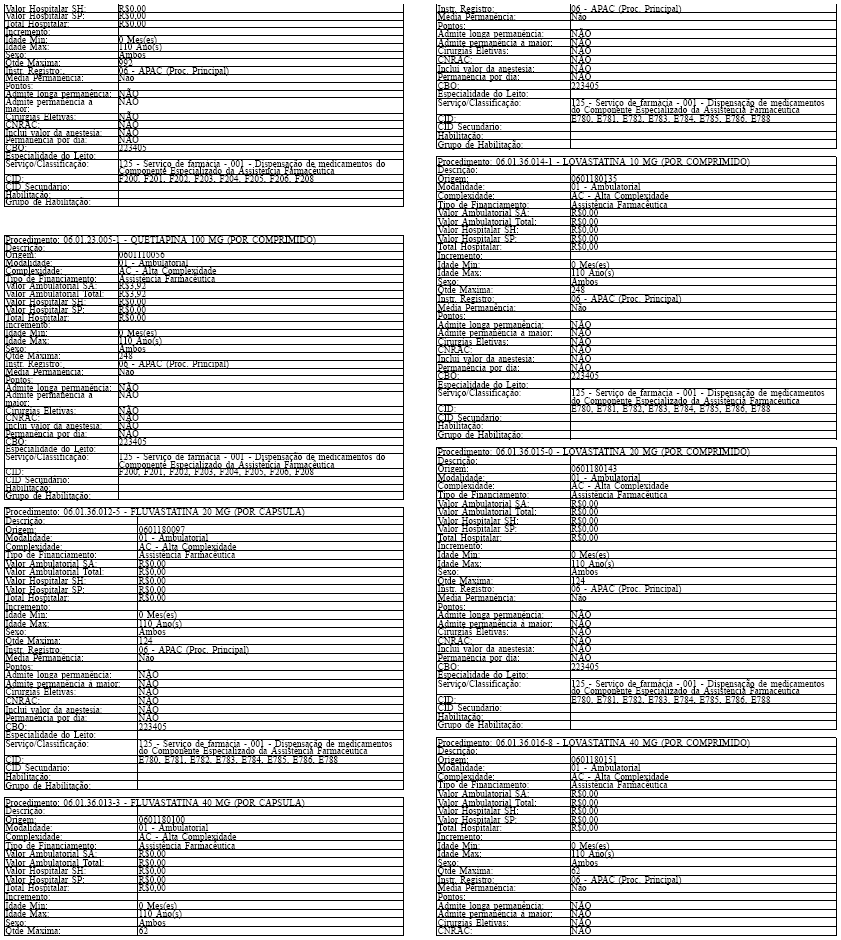
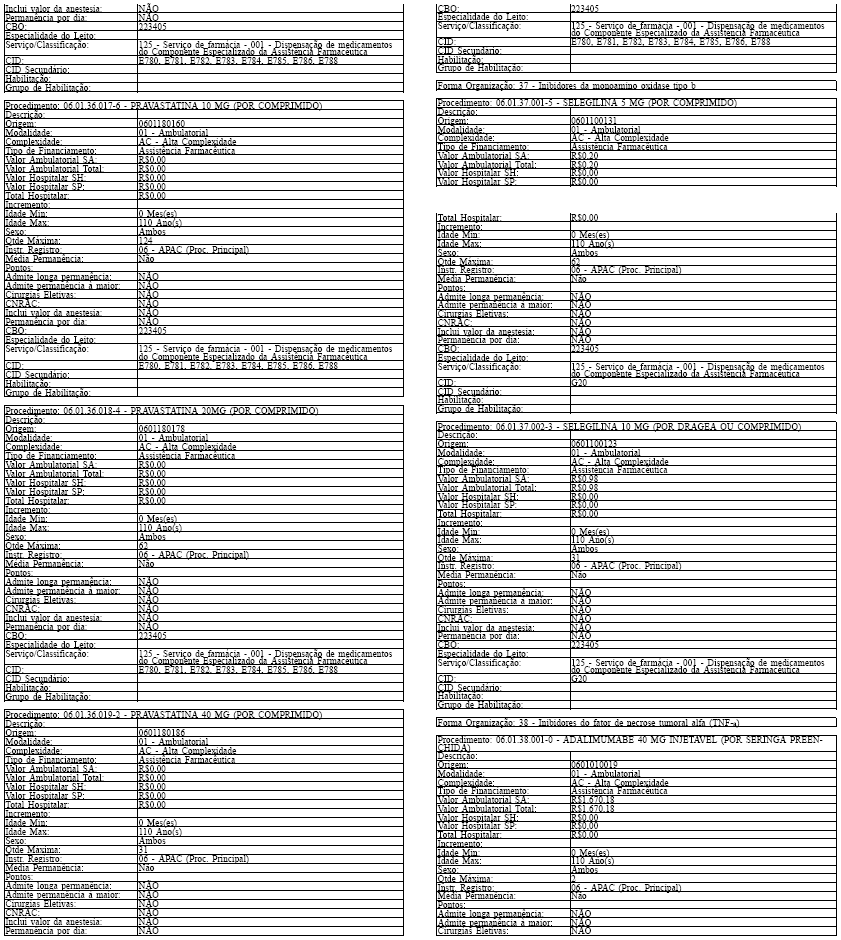
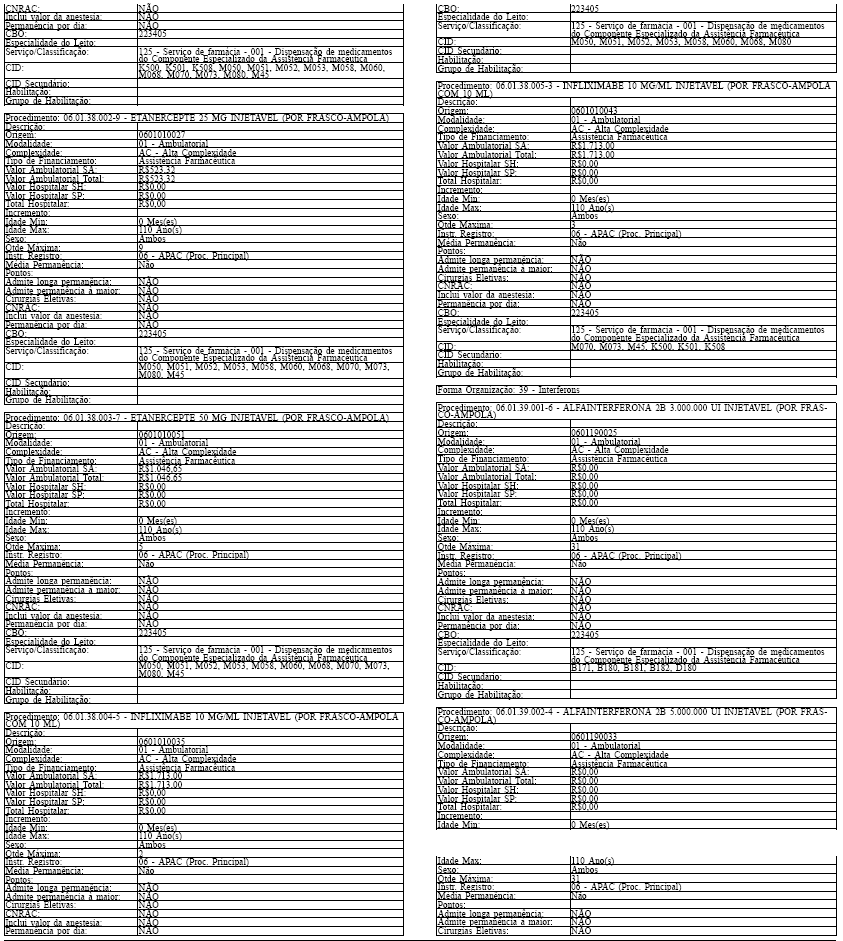
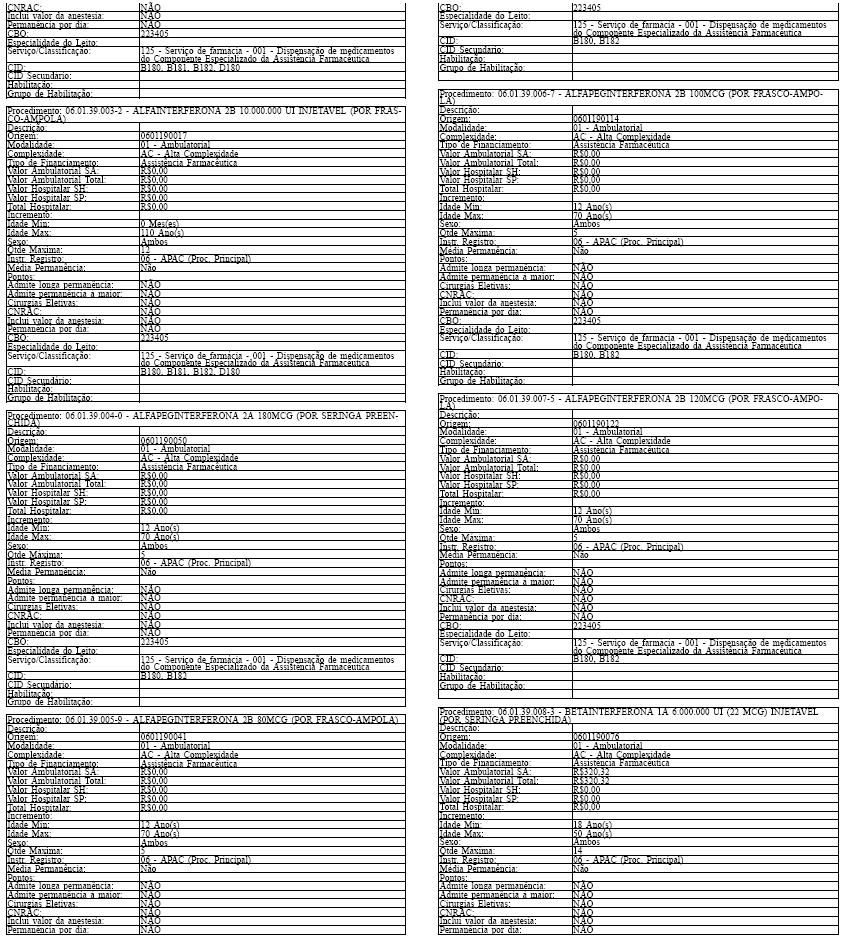
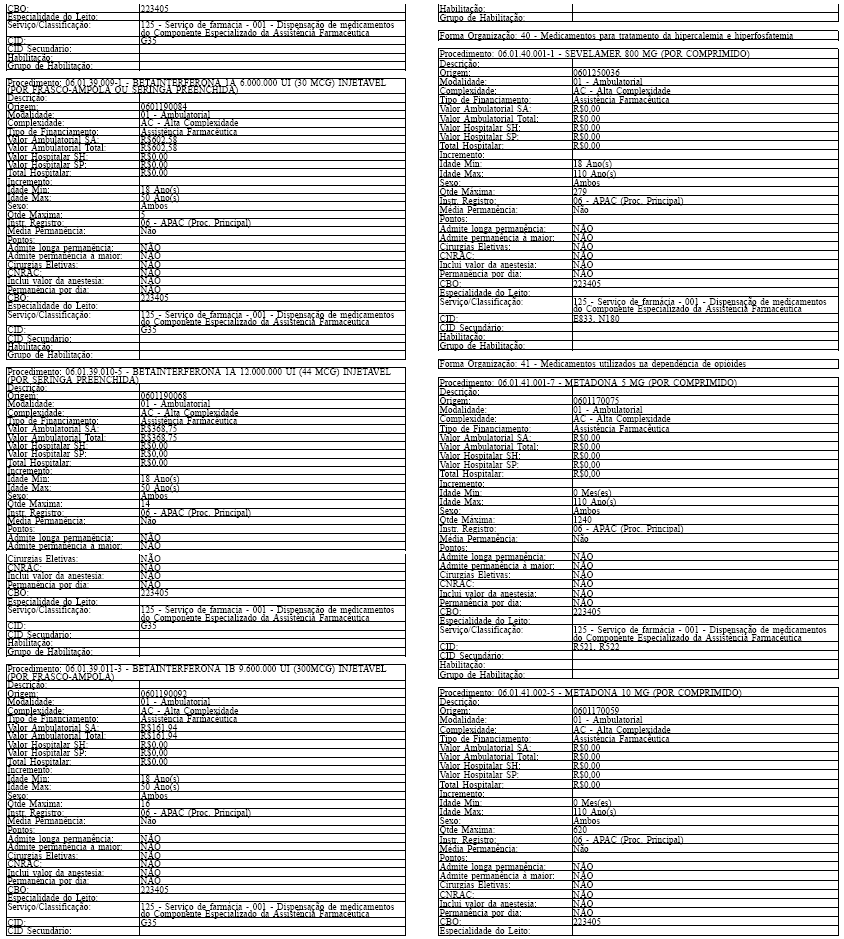
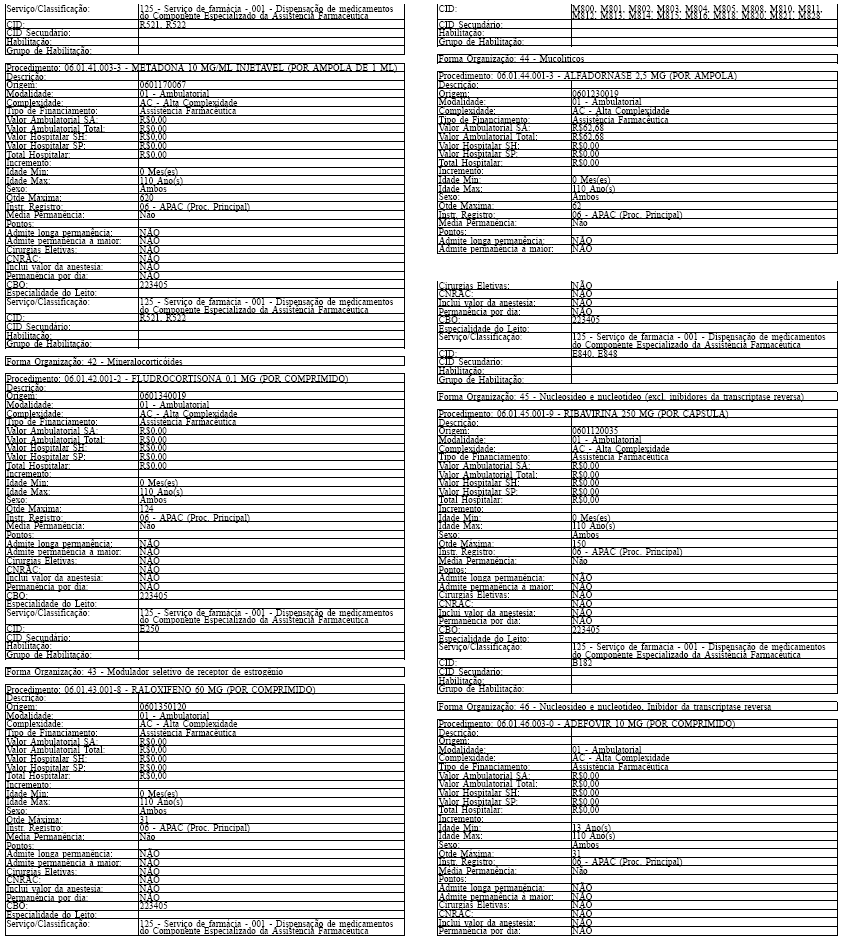
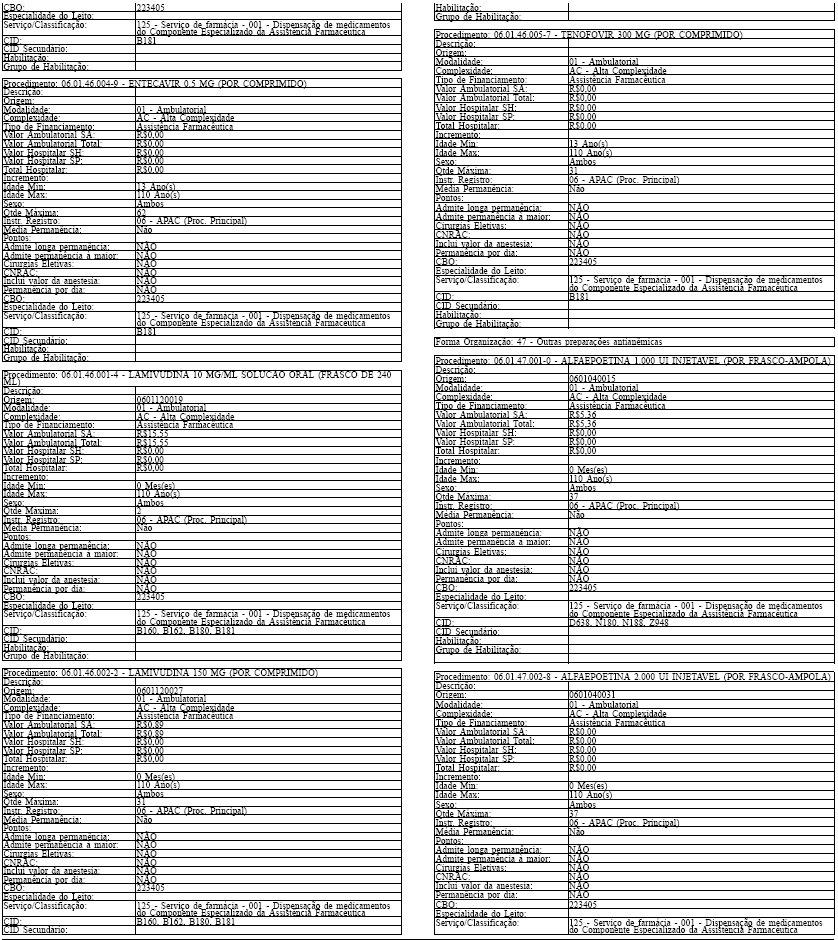
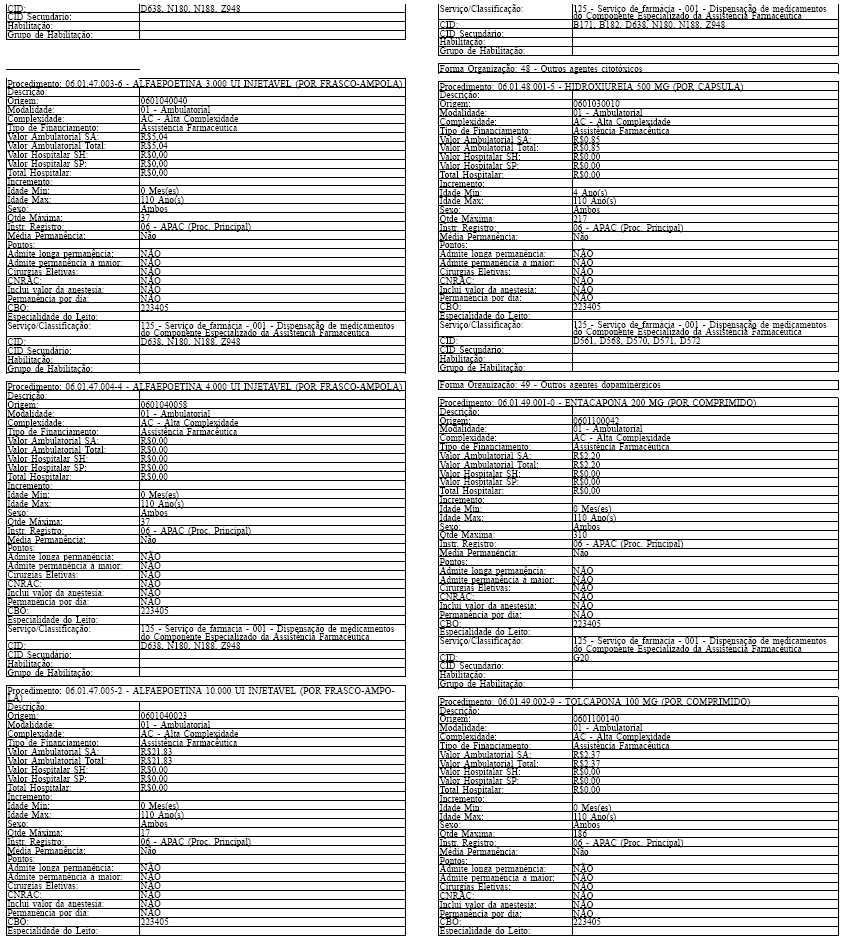
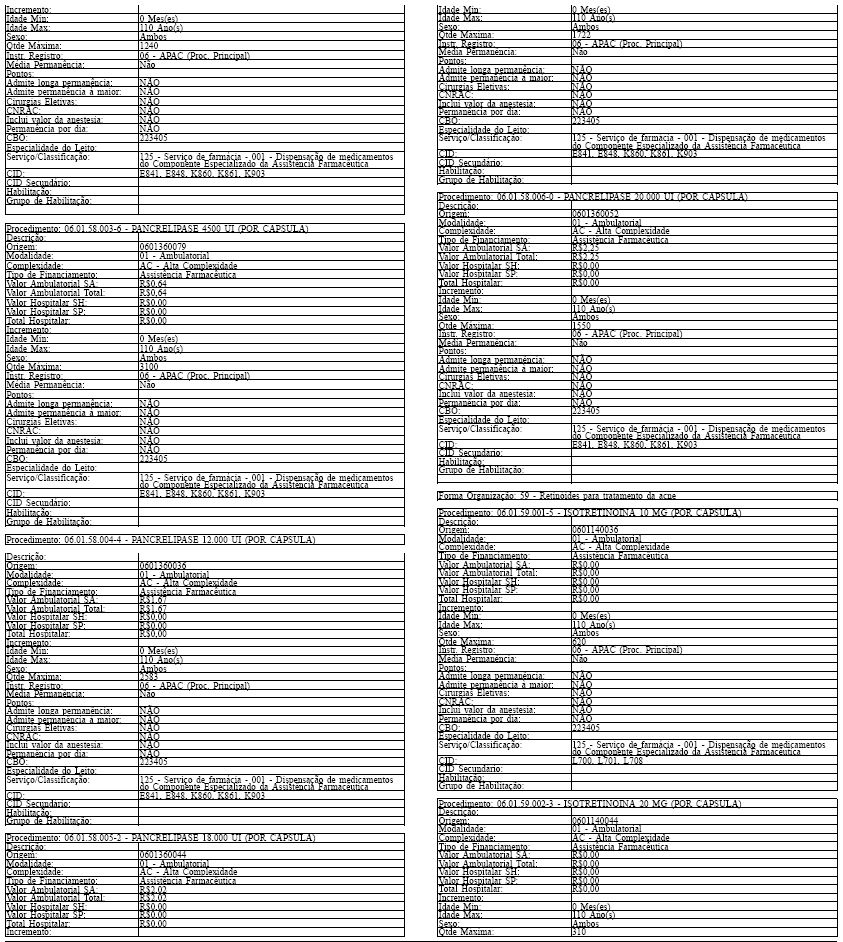
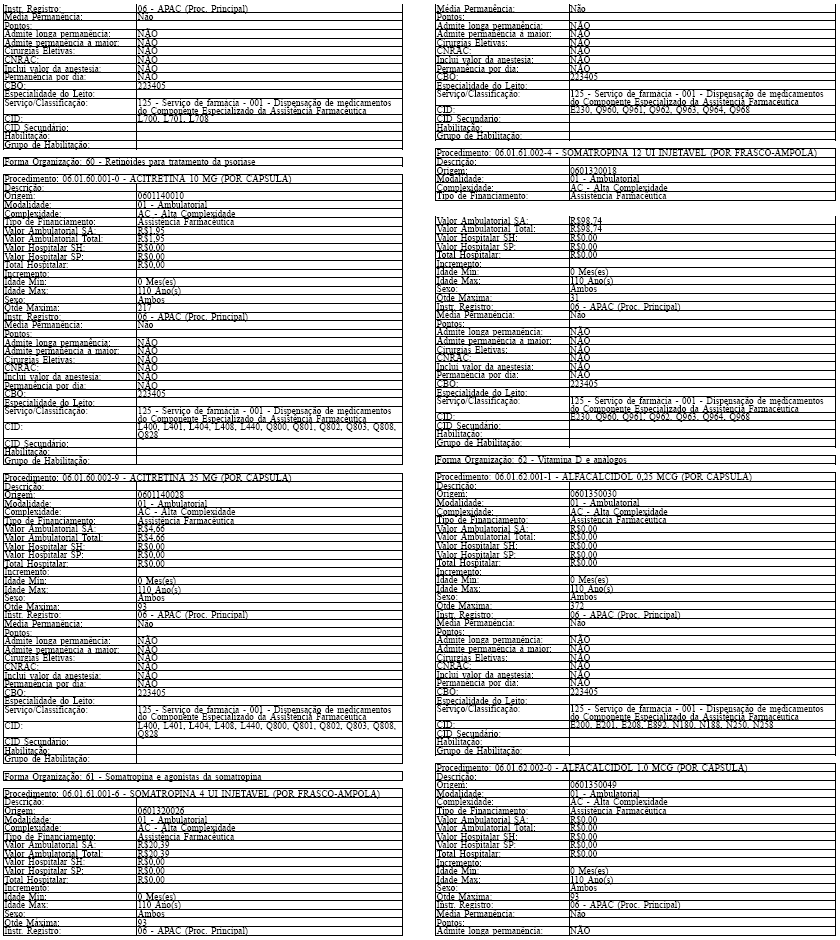

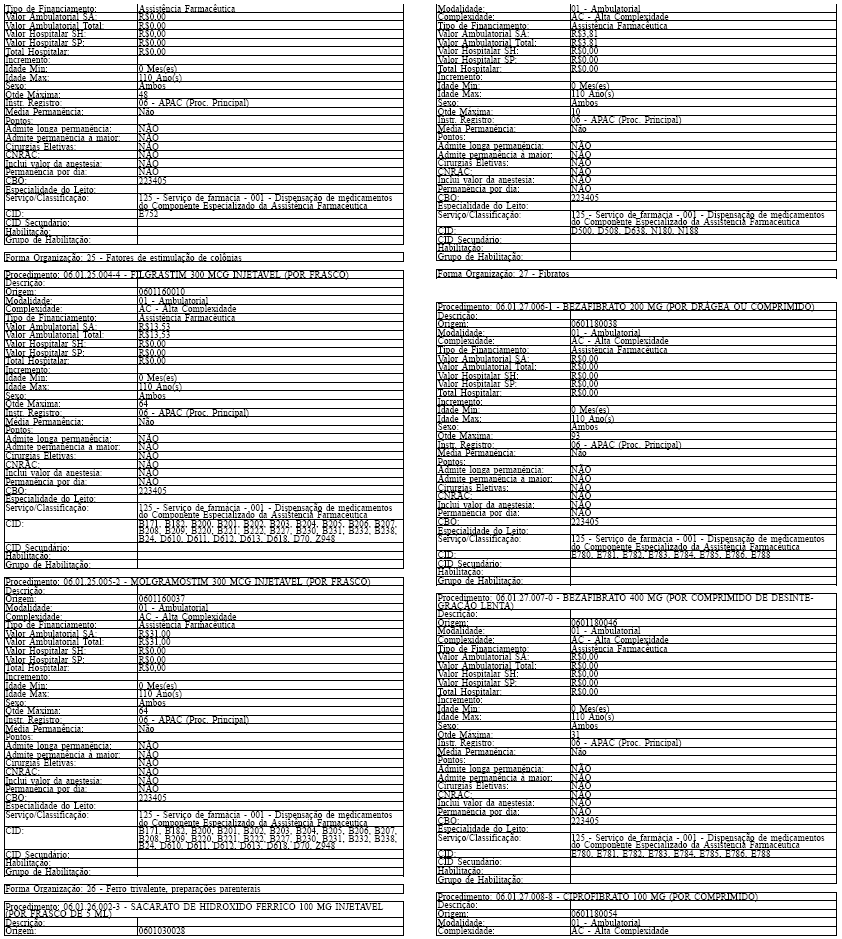
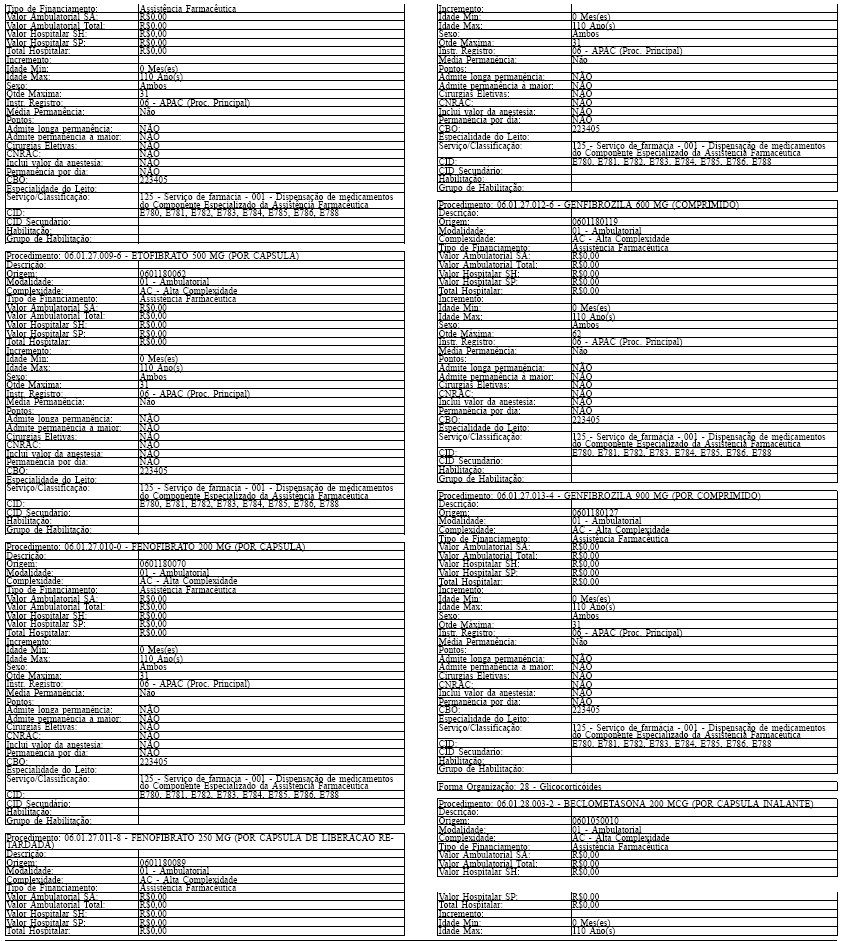


LAUDO PARA SOLICITAÇÃO, AVALIAÇÃO E AUTORIZAÇÃO DE MEDICAMENTOS DO COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA
INSTRUÇÕES DE PREENCHIMENTO
SOLICITAÇÃO DO MEDICAMENTO
Campo 1 - Nome do Paciente: preencher com o nome completo do paciente sem abreviaturas.
Campo 2 - Cartão Nacional de Saúde (CNS): preencher com o número do CNS do paciente.
Campo 3 - Nome do estabelecimento do médico solicitante: preencher com o nome fantasia do estabelecimento de saúde ao qual o médico solicitante está vinculado e que originou a solicitação de medicamento(s).
Campo 4- Cadastro Nacional de Estabelecimentos de Saúde (CNES): preencher com o código identificador do estabelecimento de saúde ao qual o médico solicitante está vinculado e que originou a solicitação de medicamento(s).
Campo 5 - Medicamento: preencher com o(s) nome(s) do(s) medicamentos(s) solicitado(s), de acordo com o descrito na Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
Campo 6 - Quantidade solicitada: preencher com a quantidade do(s) medicamento(s) solicitado(s) para cada mês de tratamento.
Campo 7 - Diagnóstico: diagnóstico da doença que motivou a solicitação do(s) medicamento(s), descrito com base na denominação da Classificação Estatística Internacional de Doenças e Problemas Relacionados à Saúde (CID-10).
Campo 8 - CID-10 Principal: preencher com o CID - 10 que corresponde à doença/lesão de base que motivou a solicitação do(s) medicamento(s).
Campo 9 - CID-10 Secundário: preencher com o CID - 10 que corresponde à doença/lesão que iniciou a cadeia de acontecimentos patológicos que conduziram diretamente a doença de base. Campo de preenchimento não obrigatório.
Campo 10 - Anamnese: histórico do paciente que vai desde os sintomas iniciais até o momento da observação clínica, realizado com base nas lembranças do paciente.
Campo 11 - Alterações laboratoriais significativas: preencher, somente se necessário, as principais alterações laboratoriais que auxiliaram/definiram a doença em questão. Campo de preenchimento não obrigatório.
Campo 12 -Tratamentos prévios: preencher com os tratamentos medicamentoso(s) e/ou não medicamentoso(s) previamente utilizados pelo paciente para a doença em questão. Campo de preenchimento não obrigatório.
Campo 13 - Condição clínica do paciente: a solicitação do medicamento deverá ser realizada pelo paciente. Entretanto, fica dispensada a obrigatoriedade da presença daquele considerado incapaz de acordo com os artigos 3º e 4º do Código Civil: os menores de dezoito anos; aqueles que, por enfermidade ou deficiência mental, não tiverem o necessário discernimento para a prática desses atos ou que não puderem exprimir sua vontade, mesmo que transitória; ébrios habituais, viciados em tóxicos, ou os que, por deficiência mental, tenham o discernimento reduzido; os excepcionais, sem desenvolvimento mental completo; os pródigos. De acordo com a avaliação clínica pelo médico, descrever se o paciente preenche os critérios, ou não, de incapacidade. Caso apresente, descrever o nome completo do responsável pelo paciente.
Campo 14 - Nome do médico solicitante: preencher com o nome do profissional que solicita o procedimento, que deve estar cadastrado no CNES do estabelecimento solicitante.
Campo 15 - Data da solicitação: preencher com a data da solicitação, registrando o dia mês e ano no formato dd/mm/aaaa.
Campo 16 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo profissional solicitante no campo 15.
Campo 17 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo profissional solicitante.
Campo 18 - Assinatura e carimbo do médico: assinatura e carimbo com número de registro no
Conselho de Classe do médico solicitante.
Campo 19 - Data de nascimento: preencher com a data de nascimento do paciente no formato dd/mm/aaaa.
Campo 20 - Altura: preencher com a altura do paciente, em metros, no dia do preenchimento.
Campo 21 - Peso: preencher com o peso do paciente, em quilogramas, no dia do preenchimento.
Campo 22 - Sexo: preencher com o sexo do paciente, assinalando com um "x" no quadro indicativo: M - Masculino ou F - Feminino.
Campo 23 - Município de residência/UF: preencher com o nome do município de residência do paciente e a sigla da unidade federativa a que pertence o município. Deve-se considerar como município de residência, o local fixo do paciente e não o de permanência temporária.
Campo 24 - Endereço: preencher com o endereço completo -rua, número, complemento e bairro.
Campo 25 - Telefone de contato: preencher com número de telefone para possíveis contatos com o paciente.
Campo 26 - Nome da mãe ou responsável: preencher com o nome completo da mãe ou do responsável pelo paciente.
Campo 27 - Nome do profissional responsável pelo preenchimento: preencher com o nome do profissional que preencheu os dados complementares do paciente em questão, o qual deve estar cadastrado no CNES do estabelecimento solicitante.
Campo 28 - Data do preenchimento: preencher com a data do preenchimento dos dados complementares no formato dd/mm/aaaa.
Campo 29 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo profissional responsável pelo preenchimento dos dados complementares do paciente no campo 28.
Campo 30 - Nº documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo profissional responsável pelo preenchimento dos dados complementares do paciente.
Campo 31 - Assinatura do responsável pelo preenchimento: assinatura do profissional responsável pelo preenchimento dos dados complementares do paciente.
AVALIAÇÃO TÉCNICA
Campo 1 - Nome do paciente: preencher com o nome completo do paciente sem abreviaturas.
Campo 2 - Cartão Nacional de Saúde (CNS): preencher com o número do CNS do paciente.
Campo 3 - Código(s)/ Medicamento(s): preencher com os medicamentos solicitados e seusrespectivos códigos da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiaisdo Sistema Único de Saúde, de preferência, na mesma ordem da solicitação.
Campo 4- CID-10 principal: preencher com o CID-10 principal descrito pelo médico solicitante.
Campo 5 - CID-10 secundário: preencher com o CID-10 secundário descrito pelo médico solicitante. Caso o médico não o descreveu, deixar este campo em branco.
Campo 6 - Deferimento: o deferimento deve ocorrer quando a solicitação de algum medicamento preenche os critérios descritos no Protocolo Clínico e Diretrizes Terapêuticas da referida doença, publicado pelo Ministério da Saúde, na versão final, e os demais parâmetros definidos do Componente Especializado da Assistência Farmacêutica. Assinalar o(s) números(s) correspondentes ao(s) medicamento(s) deferido(s).
Campo 7 - Devolução: a devolução caracteriza-se pela ausência de informação ou de documentos/exames ou preenchimento incorreto da solicitação do medicamento que impedem a plenitude da análise. Deve-se assinalar qual o motivo da devolução e o(s) número(s) correspondente(s) ao(s) medicamento(s) devolvido(s), considerando as seguintes definições: Preenchimento incompleto: assinalar quando há falta de preenchimento de algum campo considerado obrigatório no campo de solicitação de medicamento(s); Preenchimento incorreto: assinalar quando em algum campo da solicitação de medicamento(s) foi descrita informação incorreta da descrita nesta Instrução; Ausência de documentação: assinalar no caso de ausência de alguma documentação exigida pelo Protocolo Clínico e Diretrizes Terapêuticas da doença em questão ou pelo Componente Especializado da Assistência Farmacêutica; Ausência de exame: assinalar no caso de ausência de algum exame exigido pelo Protocolo Clínico e Diretrizes Terapêuticas da doença em questão; Outros: assinalar quando o motivo de devolução não se enquadrar nos demais parâmetros descritos acima
Campo 8 - Especificação: descrever, se necessário, informações complementares que auxiliem no esclarecimento do motivo da devolução.
Campo 9 - Indeferimento: o indeferimento caracteriza-se pela negativa da solicitação do(s)
medicamento(s), seja por não preencher os critérios estabelecidos pelo Protocolo Clínico e Diretrizes
Terapêuticas da referida doença, publicado pelo Ministério da Saúde, na versão final, e/ou os demais
parâmetros definidos no Componente Especializado da Assistência Farmacêutica. Deve-se assinalar qual
o motivo da devolução e o(s) número(s) correspondente(s) ao(s) medicamento(s) devolvido(s), quando
necessário, considerando as seguintes definições: Não preenche critérios do Protocolo Clínico e Diretrizes
Terapêuticas: assinalar quando a solicitação de medicamento(s) não preenche os critérios estabelecidos
no Protocolo Clínico e Diretrizes Terapêuticas, devido a condição clínica/laboratorial do
paciente ou por não possuir indicação do(s) referido(s) medicamento(s), no momento da solicitação;
Medicamento não padronizado: assinalar quando há solicitação de medicamento(s) não padronizado no
Componente Especializado da Assistência Farmacêutica; CID-10 não padronizado: assinalar no caso que
o CID-10 Primário, descrito pelo médico solicitante, não está padronizado no Componente Especializado
da Assistência Farmacêutica; Outros: assinalar quando o motivo de indeferimento não se enquadrar nos
demais parâmetros descritos acima.
Campo 10 - Especificação: descrever, se necessário, informações complementares que auxiliem a esclarecer o motivo do indeferimento.
Campo 11 - Nome do avaliador: preencher com o nome completo do avaliador.
Campo 12 - Data da avaliação: preencher com a data da avaliação no formato dd/mm/aaaa.
Campo 13 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo avaliador no campo 43.
Campo 14 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo a v a l i a d o r.
Campo 15 - Assinatura e Carimbo do avaliador: assinatura e carimbo com número de registro no Conselho de Classe do médico solicitante.
A U TO R I Z A Ç Ã O
Campo 1 - Autorização: assinalar se a solicitação de um ou mais medicamentos, previamente deferidos pelo avaliador, poderá ser autorizada. Assinalar o(s) números(s) correspondentes ao(s) medicamento(s) autorizado(s).
Campo 2 - Especificação: descrever, se necessário, informações complementares que auxiliem a esclarecer o motivo da não autorização ou demais parâmetros que justificam alguma alteração.
Campo 3 - Número da Autorização de Procedimento de Alto Custo (APAC): Descrever o número de APAC (Autorizações de Procedimento de Alta Complexidade/Custo no Sistema de Informações Ambulatoriais do SUS - SIA/SUS) gerado.
Campo 4 - Vigência: Descrever o período de vigência da APAC.
Campo 5 - Nome do autorizador: preencher com o nome do autorizador.
Campo 6 - Data da autorização: preencher com a data da autorização, registrando o dia, mês e ano no formato dd/mm/aaaa.
Campo 7 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo autorizador no campo 50.
Campo 8 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo autorizador
Campo 9 - Assinatura e carimbo do autorizador: assinatura e carimbo do autorizador

Aprova o Componente Especializado da Assistência Farmacêutica.
O MINISTRO DE ESTADO DA SAÚDE, no uso das atribuições que lhe conferem os incisos I e II do parágrafo único do art. 87 da Constituição, e
Considerando as diretrizes estabelecidas pela Política Nacional de Medicamentos, constante da Portaria nº 3.916/GM, de 30 de novembro de 1998;
Considerando os princípios e eixos estratégicos definidos pela Política Nacional de Assistência Farmacêutica aprovada pela Resolução nº 338, de 2004, do Conselho Nacional de Saúde;
Considerando as Portarias nº 399/GM, de 22 de fevereiro de 2006, que Divulga o Pacto pela Saúde e nº 204/GM, de 29 de janeiro de 2007, que regulamenta o financiamento e a transferência dos recursos federais na forma de blocos de financiamento;
Considerando a necessidade de aprimorar os instrumentos e estratégias que asseguram e ampliam o acesso da população aos serviços de saúde, incluído o acesso aos medicamentos em estreita relação com os princípios da Constituição e da organização do Sistema Único de Saúde; e
Considerando a pactuação na reunião da Comissão Intergestores Tripartite de 24 de setembro de 2009, resolve:
Art. 1º Regulamentar e aprovar, no âmbito do Sistema Único de Saúde, o Componente Especializado da Assistência Farmacêutica como parte da Política Nacional de Assistência Farmacêutica, integrante do Bloco de Financiamento da Assistência Farmacêutica, conforme definido no Capítulo I desta Portaria.
Art. 2º Alterar a denominação do Componente de Medicamentos de Dispensação Excepcional descrito no inciso III, art. 24º, seção IV, da Portaria nº 204/GM, de 29 de janeiro de 2007, para Componente Especializado da Assistência Farmacêutica.
Art. 3º Alterar a denominação do Subgrupo 01 -Medicamentos de Dispensação Excepcional do Grupo 06 - Medicamentosda Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde, para Componente Especializado da Assistência Farmacêutica, que deverá ser utilizado pelos gestores para fins de cadastro da Produção Ambulatorial.
Art 4º Alterar a denominação da classificação 001 -Dispensação de Medicamentos Excepcionais/ Especiais do Código de Serviço 125 - Serviço de Farmácia da Tabela de Serviços/Classificações do Sistema de Cadastro Nacional de Estabelecimentos de Saúde (SCNES), descrito no Anexo I da Portaria nº 154/SAS, de 18 de março de 2008, para Dispensação de Medicamentos do Componente Especializado da Assistência Farmacêutica.
Art 5º Cabe ao Departamento de Regulação, Avaliação e Controle de Sistemas (DRAC), da Secretaria de Atenção à Saúde (SAS) do Ministério da Saúde, providenciar, junto ao Departamento de Informática do SUS (DATASUS/SE/MS), as medidas necessárias para que sejam efetivadas nos Sistemas de Informações, as adequações definidas nesta Portaria.
Art. 6º Caberá à Secretaria de Ciência, Tecnologia e Insumos Estratégicos do Ministério da Saúde editar normas complementares referentes à operacionalização do Componente Especializado da Assistência Farmacêutica, observadas as pactuações na Comissão Intergestores Tripartite (CIT).
Art. 7º Definir que os recursos orçamentários de que trata esta Portaria corram por conta da funcional programática 10303.1293.4705.0001 do orçamento do Ministério da Saúde.
CAPÍTULO I - DA DEFINIÇÃO
Art. 8º O Componente Especializado da Assistência Farmacêutica é uma estratégia de acesso a medicamentos no âmbito doSistema Único de Saúde, caracterizado pela busca da garantia da integralidade do tratamento medicamentoso, em nível ambulatorial, cujas linhas de cuidado estão definidas em Protocolos Clínicos e Diretrizes Terapêuticas publicados pelo Ministério da Saúde.
Parágrafo único. O acesso aos medicamentos que fazem parte das linhas de cuidado para as doenças contempladas no âmbito deste Componente será garantido mediante a pactuação entre a União, estados, Distrito Federal e municípios, conforme as diferentes responsabilidades definidas nesta Portaria.
CAPÍTULO II - DA ORGANIZAÇÃO
Art. 9º Os medicamentos que fazem parte das linhas de cuidado para as doenças contempladas neste Componente estão divididos em três grupos com características, responsabilidades e for-mas de organização distintas.
Grupo 1 - Medicamentos sob responsabilidade da União
Grupo 2 - Medicamentos sob responsabilidade dos Estados e Distrito Federal
Grupo 3 - Medicamentos sob responsabilidade dos Municípios e Distrito Federal
Art. 10. Os grupos foram constituídos considerando os seguintes critérios gerais:
I - complexidade da doença a ser tratada ambulatorialmente;
II - garantia da integralidade do tratamento da doença no âmbito da linha de cuidado;
III - manutenção do equilíbrio financeiro entre as esferas de gestão.
Art. 11. O Grupo 1 foi constituído sob os seguintes critérios:
I -maior complexidade da doença a ser tratada ambulatorialmente;
II - refratariedade ou intolerância a primeira e/ou a segunda linha de tratamento;
III - medicamentos que representam elevado impacto financeiro para o Componente;
IV - medicamentos incluídos em ações de desenvolvimento produtivo no complexo industrial da saúde.
Art. 12. O Grupo 2 foi constituído sob os seguintes critérios:
I - menor complexidade da doença a ser tratada ambulatorialmente em relação aos elencados no Grupo 1;
II - refratariedade ou intolerância a primeira linha de tratamento.
Art. 13. O Grupo 3 foi constituído sob os seguintes critérios:
I - fármacos constantes na Relação Nacional de Medicamentos Essenciais vigente e indicados pelos Protocolos Clínicos e Diretrizes Terapêuticas, publicados na versão final pelo Ministério da Saúde, como a primeira linha de cuidado para o tratamento das doenças contempladas neste Componente.
Art. 14. O elenco de medicamentos em cada grupo está descrito nos Anexos I, II e III desta Portaria.
Parágrafo único. Os medicamentos deste Componente deverão ser autorizados somente para as doenças (descritas de acordo com o CID-10) constantes no Anexo IV a esta Portaria.
Art. 15. Os medicamentos dos Grupos1e2 sob responsabilidade da União, Estados e Distrito Federal compõem o Grupo 06,Subgrupo 01 da Tabela de Procedimentos, Medicamentos, Órteses,Próteses e Materiais Especiais do Sistema Único de Saúde, na forma e redação estabelecidas no Anexo IV a esta Portaria.
§ 1º Os atributos idade mínima, idade máxima, sexo, quantidade máxima e CID-10 da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde foram estabelecidos de acordo com os critérios estabelecidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
§ 2º O atributo quantidade máxima foi definido considerando os meses com 31 dias. Para os meses com até 30 dias, a quantidade máxima autorizada será diretamente proporcional a quantidade de dias do mês correspondente.
Art. 16. As formas de organização dos procedimentos do Grupo 06, Subgrupo 01, da Tabela de Procedimentos, Medicamentos,Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde foram redefinidas segundo os critérios de classificação da Anatomical Therapeutic Chemical (ATC) da Organização Mundial da Saúde.
§ 1º Fármacos da mesma forma de organização não deverão ser autorizados para uma mesma doença no mesmo período de vigência da APAC (Autorização de Procedimentos Ambulatoriais), exceto nos casos de recomendação dos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
§ 2º Fármacos da mesma forma de organização poderão ser autorizados para doenças diferentes no mesmo período de vigência da APAC, exceto para a forma de organização dos inibidores do fator de necrose tumoral alfa.
Art. 17. Cabe a esfera de gestão responsável, a seleção dos medicamentos entre as formas de organização da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiaisdo Sistema Único de Saúde que define os procedimentos dos Grupos 1 e 2, desde que garantidas as linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde.
Parágrafo único. A não disponibilização de medicamentos no âmbito deste Componente não garante a integralidade do tratamento, provocando desequilíbrio financeiro, devendo os gestores do SUS, em pactuação na CIT, promover ações que restabeleçam a garantia do acesso aos medicamentos estabelecidos nas linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde e o equilíbrio financeiro.
Art. 18. A incorporação, exclusão ou substituição de medicamentos ou ampliação de cobertura para medicamentos já padronizados no âmbito deste Componente, ocorrerá mediante os critérios estabelecidos pela Comissão de Incorporação de Tecnologias do Ministério da Saúde (CITEC/MS), conforme ato normativo específico e pactuação na CIT.
§ 1º O impacto orçamentário das incorporações ou ampliação de cobertura para medicamentos já incorporados será calculado pelo Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde, visando auxiliar o processo de tomada de decisão a partir da análise da incorporação pela CITEC/MS e a pactuação no âmbito da CIT.
§ 2º A responsabilidade pelo financiamento das incorporações (de novos medicamentos, de ampliação de cobertura para medicamentos já incorporados e incorporações de novas concentrações e/ou apresentações farmacêuticas) deverá ser pactuada no âmbito da CIT, respeitando-se a manutenção do equilíbrio financeiro entre as esferas de gestão e a garantia da linha de cuidado da doença.
Art. 19. A incorporação efetiva de um medicamento nos Grupos 1, 2 e 3 deste Componente ocorrerá somente após a publicação na versão final do Protocolo Clínico e Diretrizes Terapêuticas específico pelo Ministério da Saúde, observadas as pactuações na CIT.
Art. 20. O Ministério da Saúde, em pactuação na CIT, poderá avaliar a transferência, em qualquer momento, de medicamentos deste Componente para outros Componentes do Bloco da Assistência Farmacêutica ou a transferência entre os Grupos 1, 2 e 3, garantindo a disponibilização desses medicamentos no âmbito do SUS e o equilíbrio financeiro entre as esferas de gestão.
Art. 21. Para os medicamentos excluídos por esta Portaria, transferidos para outros Componentes ou que posteriormente possam ser excluídos do elenco deste Componente por meio de Portarias específicas, será considerado o prazo de 120 dias a partir da publicação da respectiva Portaria, paraapresentação das APAC no Sistema de Informações Ambulatoriais do Sistema Único de Saúde (SIA/SUS), geradas a partir da dispensação.
Art. 22. Os medicamentos do Grupo 3 são de responsabilidade dos Municípios e do Distrito Federal e compõem parte do Elenco de Referência Nacional do Componente Básico da Assistência Farmacêutica regulamentado por ato normativo específico, devendo ser disponibilizados para a garantia das linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
Art. 23. Foram excluídos os seguintes procedimentos do Grupo 06, Subgrupo 01 da Tabela de
Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde:

Art. 24. Os medicamentos do Grupo 06, Subgrupo 01, da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde relacionados abaixo
foram transferidos para o Componente Básico da Assistência Farmacêutica, considerando o art. 9º desta
Portaria:

CAPÍTULO III - DA EXECUÇÃO
Art. 25. A execução do Componente envolve as etapas de solicitação, avaliação, autorização, dispensação dos medicamentos e renovação da continuidade do tratamento.
Parágrafo único. Os medicamentos do Grupo 3 são regulamentados no âmbito do Componente Básico da Assistência Farmacêutica em ato normativo específico.
Art. 26. Para os medicamentos constantes dos Grupos 1 e 2, a execução é descentralizada às Secretarias Estaduais de Saúde, devendo ser realizada de acordo com os critérios definidos nesta Portaria.
Art. 27. A solicitação, dispensação e renovação da continuidade do tratamento deverão ocorrer somente em estabelecimentos de saúde vinculados às unidades públicas designados pelos gestores estaduais.
Art. 28. A solicitação, dispensação e a renovação da continuidade do tratamento poderão ser descentralizadas junto à rede de serviços públicos dos municípios mediante pactuação entre os gestores estaduais e municipais, desde que respeitado o disposto no art. 26 desta Portaria, os critérios legais e sanitários vigentes e os demais critérios de execução deste Componente.
Art. 29. As Secretarias Estaduais de Saúde deverão manter os Municípios informados sobre a sistemática de execução deste Componente e os critérios de acesso aos medicamentos dos Grupos 1 e 2.
A - Da solicitação
Art. 30. A solicitação de medicamentos corresponde ao pleito do paciente ou seu responsável na unidade designada pelo gestor estadual conforme art. 27 desta Portaria. Para a solicitação dos medicamentos serão obrigatórios os seguintes documentos do paciente:
I - cópia do Cartão Nacional de Saúde (CNS);
II - cópia de documento de identidade - caberá ao responsável pelo recebimento da solicitação atestar a autenticidade de acordo com o documento original;
III - Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido;
IV - prescrição médica devidamente preenchida;
V - documentos exigidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado; e
VI - cópia do comprovante de residência.
Art. 31. No processo de solicitação, o paciente poderá designar representante(s) para a retirada do medicamento. Para o cadastro de representante(s) serão exigidos os seguintes documentos, que deverão ser apresentados e inseridos junto com os documentos para a solicitação: declaração autorizadora, nome e endereço completos, cópia do documento de identidade e número de telefone da pessoa autorizada.
Parágrafo único. Fica dispensada a presença dos pacientes aqueles considerados incapazes, conforme arts. 3º e 4º do Código Civil, e devidamente caracterizados no LME, pelo médico prescritor.
Art. 32. Cada usuário deverá ter apenas um único cadastro no Componente, independente do número de LME vigentes.
B - Da avaliação
Art. 33. O avaliador deverá ser um profissional de saúde com ensino superior completo, registrado em seu devido conselho de classe e designado pelo gestor estadual.
Art. 34. Para a avaliação técnica da solicitação dos medicamentos, deverão ser considerados os documentos exigidos no art. 30, observando-se:
I - Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido, de acordo com as instruções apresentadas no Anexo V a esta Portaria;
II - prescrição médica contendo as informações exigidas na legislação vigente; e
III - todos os documentos exigidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado.
Parágrafo único. A análise técnica da solicitação deve ser realizada considerando os campos referentes à avaliação descrita no LME, conforme as instruções apresentadas no Anexo V a esta Portaria.
C - Da autorização
Art. 35. O autorizador deverá ser um profissional de nível superior completo, preferencialmente da área da saúde, designado pelo gestor estadual.
Art. 36. A autorização do LME deverá ser efetivada somente após o deferimento da avaliação realizada de acordo com o art. 33 e art. 34 desta Portaria.
D - Da dispensação
Art. 37. A dispensação do medicamento deverá ser efetivada somente após a autorização realizada de acordo com o art. 35 e art. 36 desta Portaria.
Art. 38. No ato da dispensação, o recibo de dispensação do medicamento deverá estar devidamente preenchido e assinado.
Parágrafo único. O Recibo de Medicamentos (RME) a ser utilizado no âmbito deste Componente deverá conter, no mínimo, os dados constantes no modelo apresentado no Anexo VI a esta Portaria.
Art. 39. Uma via do LME, os recibos de dispensação dos medicamentos e os documentos descritos no art. 30 desta Portaria deverão ser mantidos em arquivo pelo prazo estabelecido na legislação em vigor.
Art. 40. A dispensação do medicamento poderá ser realizada para mais de um mês de competência, dentro do limite de vigência da APAC e respeitadas as exigências legais.
Art. 41. O processamento mensal da APAC no Sistema SIA/SUS deverá ser efetivado somente a partir da emissão do recibo de dispensação do medicamento contendo a assinatura do usuário ou seu representante.
Art. 42. A interrupção do fornecimento por abandono do tratamento deverá ser realizada quando
o paciente ou representante não retirar o medicamento por três meses consecutivos e não tiver ocorrido
o fornecimento antecipado, previsto no art. 40 desta Portaria.
Art. 43. O Sistema SIA/SUS exercerá crítica para todos os medicamentos dos Grupos 1 e 2 doComponente, conforme os atributos da Tabela de Procedimentos, Medicamentos, Órteses, Próteses eMateriais Especiais do Sistema Único de Saúde, apresentada no Anexo IV a esta Portaria.
E - Da renovação
Art. 44. Para a renovação da continuidade do tratamento serão obrigatórios os seguintes documentos do paciente:
I - Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente Especializado da Assistência Farmacêutica (LME), adequadamente preenchido, de acordo com as instruções apresentadas no Anexo V desta Portaria;
II - prescrição médica contendo as informações exigidas na legislação vigente; e
III - todos os documentos para monitoramento do tratamento estabelecidos nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final pelo Ministério da Saúde, conforme a doença e o medicamento solicitado.
CAPÍTULO IV
DA PROGRAMAÇÃO, AQUISIÇÃO, ARMAZENAMENTO E DISTRIBUIÇÃO
Art. 45. A responsabilidade pela programação, armazenamento e distribuição dos medicamentos dos Grupos 1A e 1B do Anexo I a esta Portaria é das Secretarias Estaduais de Saúde, sendo a responsabilidade pela aquisição dos medicamentos do Grupo 1A do Ministério da Saúde e dos medicamentos do Grupo 1B das Secretarias Estaduais de Saúde.
Art. 46. A responsabilidade pela programação, aquisição, armazenamento e distribuição dos medicamentos do Grupo 2 do Anexo II desta Portaria é de responsabilidade das Secretarias Estaduais de Saúde.
Art. 47. A responsabilidade pela programação, aquisição, armazenamento e distribuição dos medicamentos do Grupo 3 é dos Municípios e está estabelecida em ato normativo específico que regulamenta o Componente Básico da Assistência Farmacêutica.
Art. 48. Na aquisição dos medicamentos dos Grupos 1 e 2, os gestores deverão observar o Preço Máximo de Venda ao Governo (PMVG) conforme regulamentação vigente da Câmara de Regulação do Mercado de Medicamentos (CMED) e os preços praticados no mercado, no sentido de obter a proposta mais vantajosa para a administração pública.
Parágrafo único. Os responsáveis pelas aquisições deverão verificar, ainda, a aplicação dos benefícios fiscais que incidem sobre os medicamentos listados nos Convênios ICMS (CONFAZ) vigentes.
CAPÍTULO V
DOS MEDICAMENTOS DE AQUISIÇÃO CENTRALIZADA PELO MINISTÉRIO DA SAÚ-DE
Art. 49. O Ministério da Saúde, as Secretarias Estaduais de Saúde e o Distrito Federal poderão pactuar a aquisição centralizada dos medicamentos pertencentes ao Grupos 1B (conforme o Anexo I) e Grupo 2 (conforme Anexo II) deste Componente, desde que seja garantido o equilíbrio financeiro entre as esferas de gestão, observando, entre outros, o benefício econômico da centralização frente às condições do mercado e os investimentos estratégicos do governo no desenvolvimento tecnológico e da capacidade produtiva junto aos laboratórios públicos e oficiais.
Art. 50. Os medicamentos a seguir identificados serão adquiridos por meio de processo centralizado
no Ministério da Saúde.


§ 1º A distribuição dos medicamentos cuja aquisição é de responsabilidade do Ministério da Saúde ocorrerá a partir da finalização dos procedimentos administrativos indispensáveis para o processo de aquisição.
§ 2º O valor desses medicamentos na Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde corresponderá a zero a partir da primeira distribuição realizada pelo Ministério da Saúde.
§ 3º Após a primeira distribuição dos medicamentos de aquisição centralizada, o Ministério da Saúde realizará o ressarcimento correspondente ao estoque estadual com base nas APAC faturadas no prazo de 180 dias, considerando os valores definidos anteriormente ao zeramento da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
Art. 51. A dispensação dos medicamentos de aquisição centralizada pelo Ministério da Saúde é de responsabilidade das Secretarias Estaduais de Saúde e deve seguir os critérios estabelecidos no Capítulo III desta Portaria.
A - Da programação anual
Art. 52. As Secretarias Estaduais de Saúde deverão encaminhar ao Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde a programação anual de cada medicamento de aquisição centralizada.
Parágrafo único. A programação anual dos medicamentos é de responsabilidade das Secretarias Estaduais de Saúde e deverá ser enviada no período de 1º a 20 de julho de cada ano, devendo considerar a média das APAC aprovadas nos seis (6) meses anteriores. Mediante apresentação de justificativa e avaliação do Ministério da Saúde, será permitido incremento de até 20% para o período.
B - Da programação trimestral
Art. 53. As Secretarias Estaduais de Saúde deverão encaminhar ao Departamento de Assistência Farmacêutica e Insumos Estratégicos do Ministério da Saúde a necessidade trimestral de cada medicamento de aquisição centralizada, conforme cronograma abaixo:
§ 1º O quantitativo a ser distribuído para o trimestre deverá considerar também a programação anual.
§ 2º A distribuição dos medicamentos seguirá o período de entrega estabelecido no cronograma abaixo:
C - Do controle e monitoramento da programação
Art. 54. A distribuição dos medicamentos adquiridos de forma centralizada pelo Ministério da Saúde terá como parâmetros a programação anual enviada pelas Secretarias Estaduais de Saúde e a continuidade e regularidade da produção registrada em APAC.
Art. 55. Após a finalização da programação anual pelas Secretarias Estaduais de Saúde para os medicamentos de aquisição centralizada pelo Ministério da Saúde, caso seja verificado que o consumo, via produção registrada em APAC, para o período anual seja inferior ao quantitativo total distribuído, a diferença será ajustada na programação seguinte.
Art. 56. Após a entrega dos medicamentos de aquisição centralizada pelo Ministério da Saúde, toda logística restante será de responsabilidade exclusiva dos Estados e do Distrito Federal.
CAPÍTULO VI - DO FINANCIAMENTO
Art. 57. O financiamento para aquisição dos medicamentos do Componente estará diretamente relacionado ao grupo em que os mesmos alocados.
Art. 58. Os medicamentos do Grupo 3 serão financiados de acordo com a regulamentação do Componente Básico da Assistência Farmacêutica, em ato normativo específico.
Art. 59. Os medicamentos pertencentes ao Grupo 2 serão financiados integralmente pelos Estados e Distrito Federal, observando o disposto no art. 48 deste Componente.
Parágrafo único. A Tabela de Procedimentos, Medicamentos, Órteses, Próteses e MateriaisEspeciais do Sistema Único de Saúde para os medicamentos do Grupo 2 terá o valor igual a zero a partir da vigência desta Portaria.
Art. 60. Os medicamentos pertencentes ao Grupo 1 serão financiados pelo Ministério da Saúde na forma de aquisição centralizada (Grupo 1A), conforme definições do Capítulo V desta Portaria, e na forma de transferência de recursos financeiros (Grupo 1B).
Art. 61. Os valores dos medicamentos financiados pelo Ministério da Saúde e adquiridos pelasSecretarias Estaduais da Saúde da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde serão calculados considerando o PMVG conforme regulamentação vigente da CMED, observando o disposto no art. 48 e terão validade a partir da vigência desta Portaria.
§ 1º Para os medicamentos que não estão sujeitos ao Coeficiente de Adequação de Preço (CAP), o PMVG será considerado como o Preço de Fábrica definido pela CMED.
§ 2º Caso o valor praticado no mercado seja inferior ao estabelecido pelo PMVG, o financiamento será calculado com base na média ponderada dos valores praticados, definidos pelos valores atualizados do Banco de Preços em Saúde ou por meio da solicitação de preço aos Estados e ao Distrito Federal.
Art. 62. Os valores dos medicamentos constantes da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde serão atualizados anualmente conforme definições de preço da CMED e preços praticados pelos Estados e ao Distrito Federal.
Parágrafo único. A periodicidade da revisão dos valores poderá ser inferior a 12 meses con-forme interesse da administração pública, observando-se a pactuação na CIT.
Art. 63. Trimestralmente, o Ministério da Saúde publicará Portaria com os valores a serem transferidos mensalmente às Secretarias Estaduais de Saúde, apurados com base na média das APAC emitidas e aprovadas conforme critérios e valores de referência indicados para o Grupo 06, Subgrupo 01da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
§ 1º O Ministério da Saúde, por meio do Departamento de Assistência Farmacêutica e Insumos Estratégicos, consolidará as informações no Sistema SIA/SUS até o último dia útil do mês subsequente a apuração da média do trimestre anterior, para publicação de Portaria com os valores a serem transferidos aos Estados.
§ 2º O Fundo Nacional de Saúde repassará aos Fundos Estaduais de Saúde, mensalmente até o décimo quinto dia e na modalidade fundo a fundo, os valores apurados e publicados, os quais deverão ser movimentados em conta específica.
Art. 64. Os recursos do Ministério da Saúde aplicados no financiamento do Grupo 1B terão como base a emissão e a aprovação das APAC emitidas pelas Secretarias Estaduais de Saúde, vinculadas à efetiva dispensação do medicamento e de acordo com os critérios técnicos definidos nesta Portaria.
CAPÍTULO VII - DO CONTROLE E MONITORAMENTO
Art. 65. A União, os Estados, o Distrito Federal e os Municípios deverão monitorar os recursos aplicados no financiamento do Componente, com vistas a ajustes que assegurem o equilíbrio da responsabilidade e a participação no financiamento entre as esferas de gestão, cujas análises devem ser sustentadas por informações sobre os preços praticados, quantidades adquiridas e número de pacientes atendidos.
Art. 66. As Secretarias Estaduais de Saúde deverão enviar mensalmente ao DATASUS, da Secretaria-Executiva do Ministério da Saúde, as informações, via APAC, dos procedimentos constantes nos Grupos 1 e 2 e selecionados pelas Secretarias Estaduais de Saúde de acordo com o art. 17 desta Portaria, observando o cronograma estabelecido pelo Ministério da Saúde em ato normativo específico.
Parágrafo único. A não emissão das APAC para os medicamentos que compõem o Grupo 2 será entendida como a não garantia da linha de cuidado sob responsabilidade do gestor estadual, podendo acarretar em novas definições no financiamento, no sentido de manter o equilíbrio financeiro entre as esferas de gestão.
Art. 67. De acordo com o art. 6º do Decreto nº 1.651, de 1995, a comprovação da aplicação dos recursos transferidos do Fundo Nacional de Saúde para os Fundos Estaduais de Saúde, na forma do Decreto nº 1.232, de 1994, que trata das transferências fundo a fundo, deverá ser apresentada ao Ministério da Saúde e as Secretarias Estaduais de Saúde, por meio de Relatório de Gestão, aprovado pelo respectivo Conselho de Saúde.
Art. 68. O Ministério da Saúde, juntamente com Estados e Municípios, deverá realizar controle, avaliação e monitoramento sistemático da organização, execução e financiamento, com vistas ao aprimoramento permanente do Componente e a garantia das linhas de cuidado definidas nos Protocolos Clínicos e Diretrizes Terapêuticas publicados na versão final, pelo Ministério da Saúde.
Parágrafo único. As Secretarias Estaduais de Saúde deverão fornecer ao Ministério da Saúde, sempre que solicitado, informações referentes à organização, a execução, ao acompanhamento e monitoramento do Componente.
Art. 69. Para o controle e monitoramento, o Ministério da Saúde disponibilizará sistema informatizado de gerenciamento e acompanhamento dos medicamentos do Componente.
§ 1º As Secretarias Estaduais de Saúde deverão adotar o sistema disponibilizado ou outro similar próprio que contemple os requisitos e informações previstos nesta Portaria.
§ 2º O Ministério da Saúde publicará ato normativo para regulamentar e definir as regras de utilização do referido sistema.
CAPÍTULO VIII
DO LAUDO PARA SOLICITAÇÃO, AVALIAÇÃO E AUTORIZAÇÃO DE MEDICAMENTOS DO COMPONENTE ESPECIALIZADO DA ASSISTÊNCIA FARMACÊUTICA
Art. 70. O Laudo para Solicitação, Avaliação e Autorização de Medicamentos do Componente
Especializado da Assistência Farmacêutica (LME) é o instrumento que deve ser utilizado para execução
deste Componente.
Art. 71. O modelo do LME que deverá ser utilizado no âmbito deste Componente e as instruções para o adequado preenchimento estão descritos no Anexo V a esta Portaria.
§ 1º O LME estará estruturado para que seja preenchido com informações sobre a solicitação, avaliação e autorização do procedimento.
§ 2º O preenchimento da solicitação deverá ser realizado pelo médico solicitante. Os campos relativos aos dados complementares do paciente poderão ser preenchidos por outro profissional, desde que cadastrado no mesmo estabelecimento de saúde do médico solicitante.
Art. 72. Para cada doença, definida de acordo com a Classificação Estatística Internacional de doenças e Problemas Relacionados à Saúde (CID-10), haverá a necessidade de preenchimento de um LME.
§ 1º Cada LME corresponderá a uma única APAC.
§ 2º Em caso de solicitação de mais de cinco medicamentos para a mesma doença (CID-10), o mesmo médico deverá preencher mais de um LME. Nesse caso, deverá ser emitido apenas um número de APAC.
§ 3º Durante o período de vigência da APAC de um LME será permitido o ajuste da solicitação da seguinte forma: substituição, inclusão ou exclusão de procedimentos para o tratamento da mesma doença (CID-10) ou alteração da quantidade solicitada pelo médico, caracterizando adequação do LME.
§ 4º Nos casos em que o medicamento não tiver indicação para utilização contínua, deverá ser emitida APAC única, que corresponderá apenas ao mês de atendimento
Art. 73. Será permitida a emissão de mais de uma APAC dentro do mesmo período de vigência, nos casos de pacientes diagnosticados com mais de uma doença (CID-10).
Art. 74. O LME terá sessenta (60) dias de validade para solicitação do medicamento, a partir de sua data de preenchimento pelo médico solicitante.
Art. 75. Para cada LME deverá ser emitido um parecer do avaliador.
Parágrafo único. Caso seja solicitado mais de um medicamento no mesmo LME, a avaliação poderá possuir mais de um parecer.
Art. 76. O LME será assinado somente pelo autorizador nos casos de deferimento de um medicamento pelo avaliador.
Art. 77. Esta Portaria entrará em vigor após noventa (90) dias da sua publicação.
Art. 78. Ficam revogadas as Portarias nº 1.259/GM, de 17 de junho de 2009, publicada no Diário Oficial da União nº 114, de 18 junho de 2009, Seção I, página 44; nº 106/GM, de 22 de janeiro de 2009, publicada no Diário Oficial nº 16, de 23 de janeiro de 2009, Seção I, página 40; nº 850/GM, de 20 de abril de 2007, publicada no Diário Oficial da União nº 77, de 23 de abril de 2007, Seção I, página 26; Portarias nº 1.320/GM, de 5 de junho de 2007, publicada no Diário Oficial da União nº 108, de 6 junho de 2007, Seção I, página 65; nº 2.577/GM, de 27 de outubro de 2006, publicada no Diário Oficial da União nº 208, de 30 outubro de 2006, Seção I, página 147; nº 3.227/GM, de 20 de dezembro de 2006, publicada no Diário Oficial da União nº 244, de 21 de dezembro de 2006, Seção I, página 76 nº 1.654/GM, de 11 de agosto de 2004, publicada no Diário Oficial da União nº 162, de 12 de agosto de 2004, Seção I, página 53; nº 971/GM, de 3 de julho de 2001, publicada no Diário Oficial da União nº 128, de 4 de julho de 2001, Seção I, página 121; nº 254/GM, de 31 de março de 1999, publicada no Diário Oficial da União nº 62, de 1º de abril de 1999, Seção I, página 10; nº 14/SCTIE, de 19 de dezembro de 2008, publicada no Diário Oficial da União nº 248, de 22 de dezembro de 2008, Seção I, página 289; nº 341/SAS, de 22 de agosto de 2001, publicada no Diário Oficial da União nº 162, de 23 de agosto de 2001, Seção I, página 50; nº 14/SAS, de 14 de janeiro de 1999, publicada no Diário Oficial da União nº 162, de 15 de janeiro de 1999, Seção I, página 10; nº 105/SAS, de 29 de março de 1999, publicada no Diário Oficial da União nº 60 de 30 de março de 1999, Seção I, página 44; nº 138/SAS, de 20 de abril de 1999, publicada no Diário Oficial da União nº 76, de 23 de abril de 1999, Seção I, página 112; nº 50/SAS, de 21 de junho de 1995, publicada no Diário Oficial da União nº 118, de 22 de junho de 1995, Seção I, página 9168; nº 112/SAS, de 6 de outubro de 1993, publicada no Diário Oficial da União nº 198, de 18 de outubro de 1993, Seção I, página 15541; e o Anexo II da Portaria nº 768/SAS, de 26 de outubro de 2006, publicada no Diário Oficial da União nº 207, de 27 de outubro de 2006, Seção I, página 91.
JOSÉ GOMES TEMPORÃO
ANEXO I
GRUPO 1A: Medicamentos com aquisição centralizada pelo Ministério da Saúde para tratamento das
doenças contempladas neste Componente.

GRUPO 1B: Medicamentos financiados com transferência de recursos financeiros pelo Ministério da
Saúde para tratamento das doenças contempladas neste Componente.


ANEXO II
GRUPO 2: Medicamentos financiados pelas Secretarias de Estado da Saúde para tratamento das doenças
contempladas neste Componente.


ANEXO III
GRUPO 3: Medicamentos cuja dispensação é de responsabilidade dos municípios e Distrito Federal para
tratamento das doenças contempladas neste Componente.


ANEXO IV
Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único
de Saúde
Grupo: 06 - Medicamentos
Sub Grupo: 01 - Componente Especializado da Assistência Farmacêutica
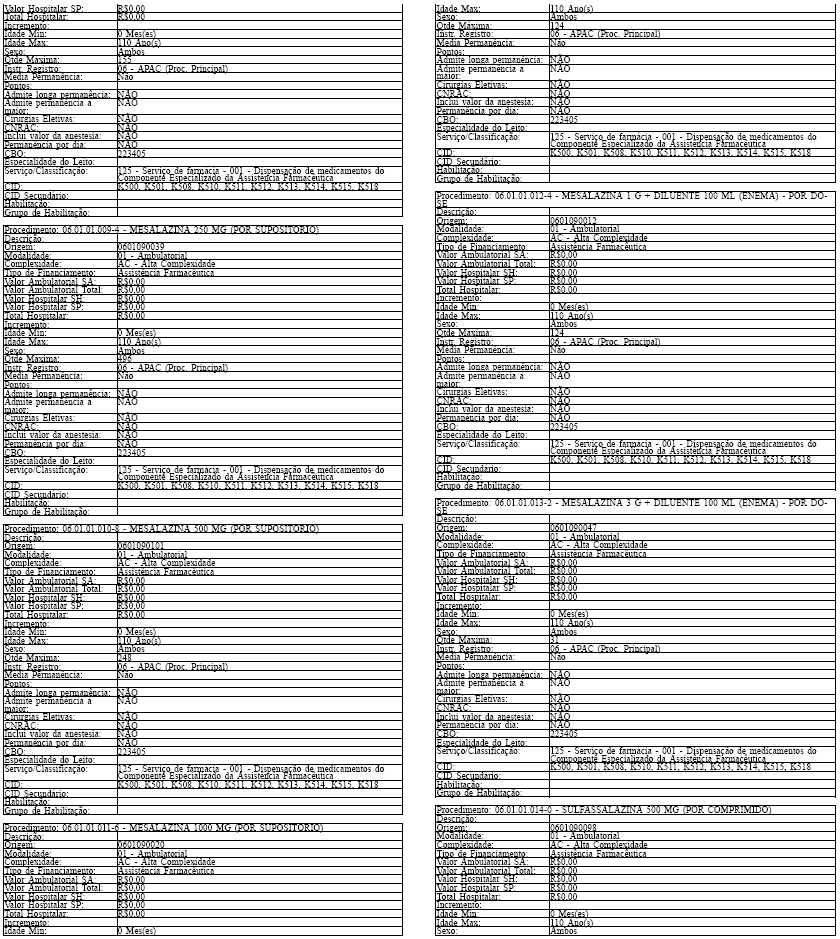
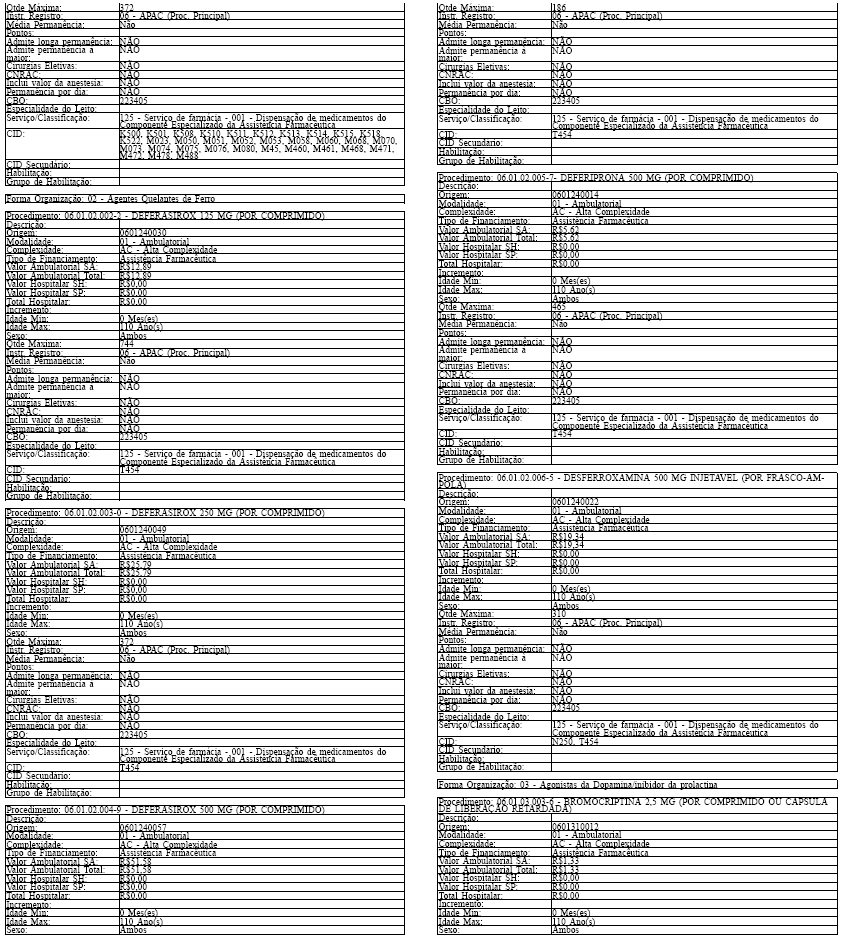
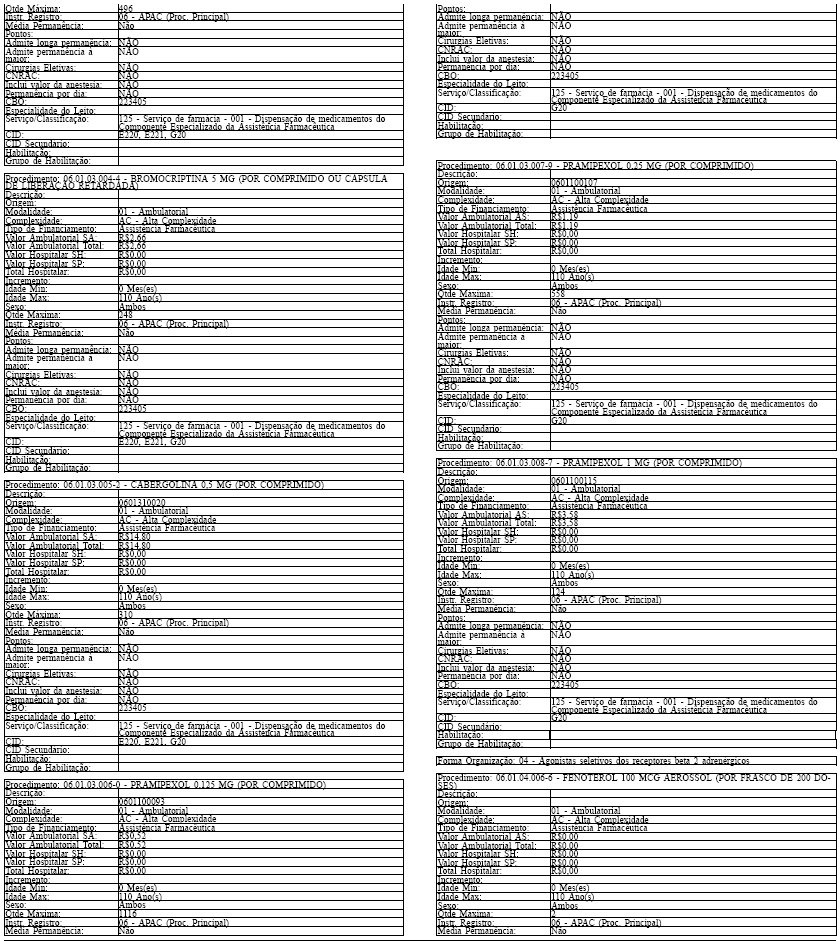
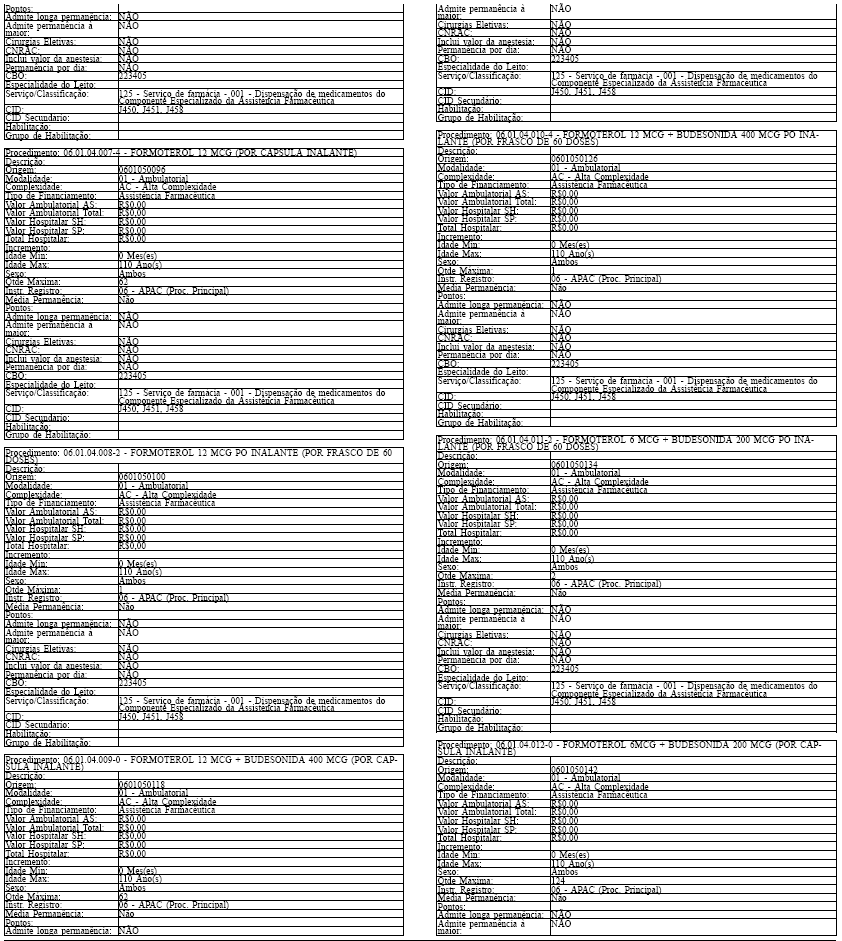
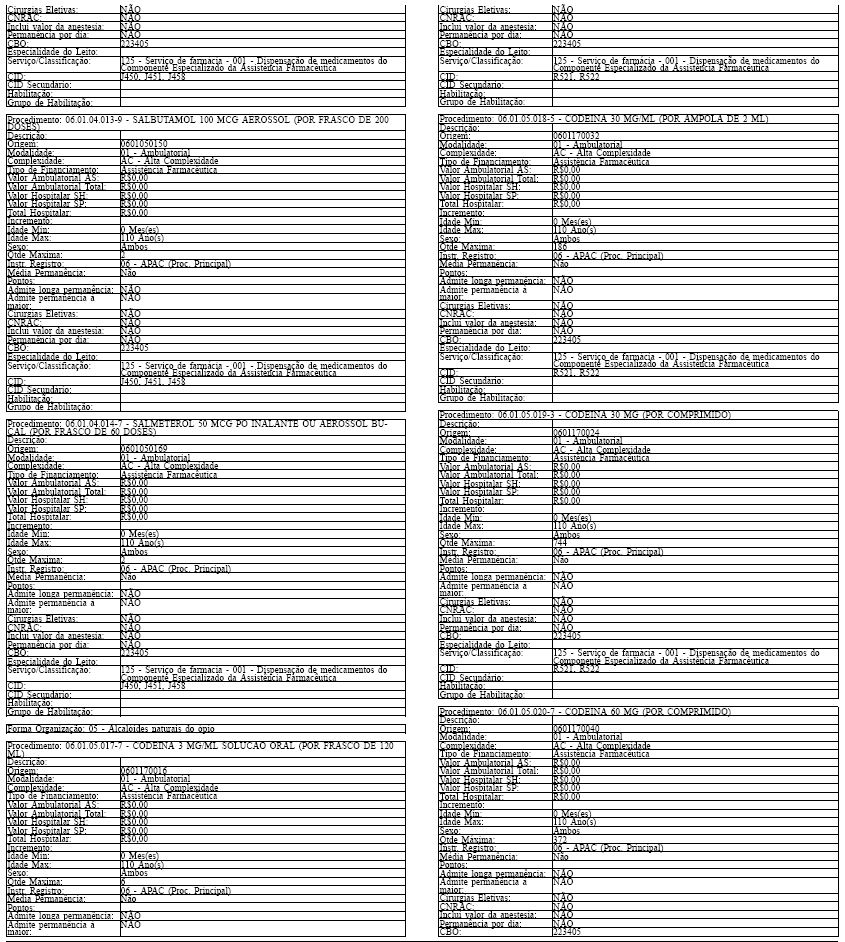
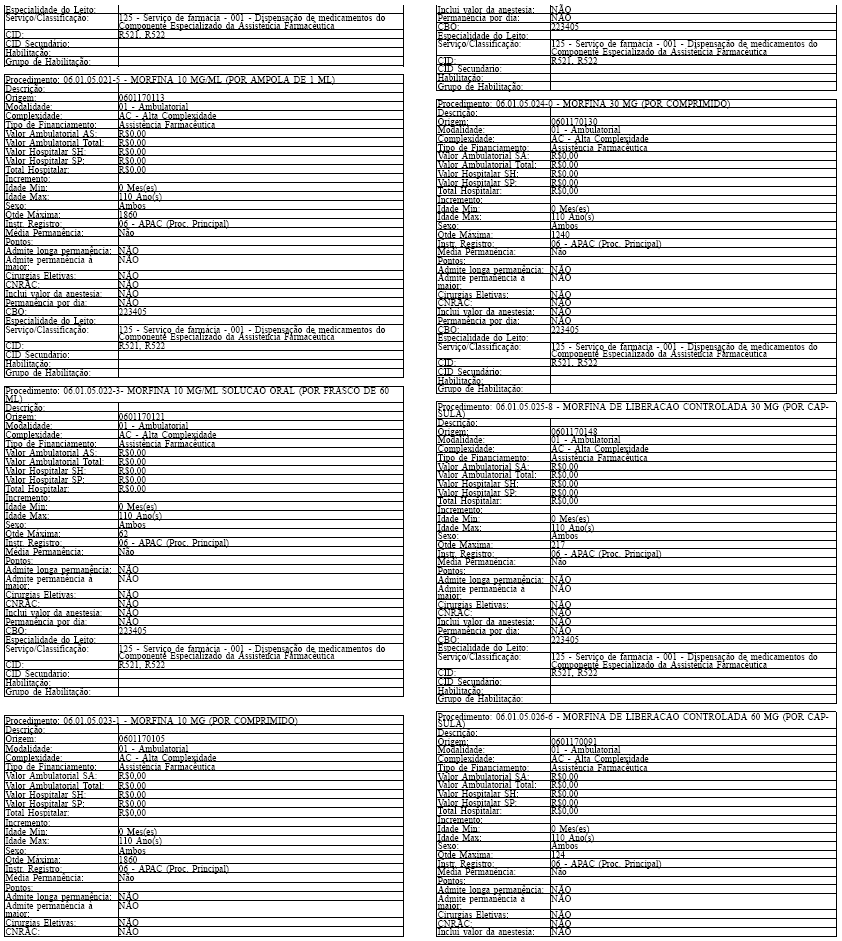
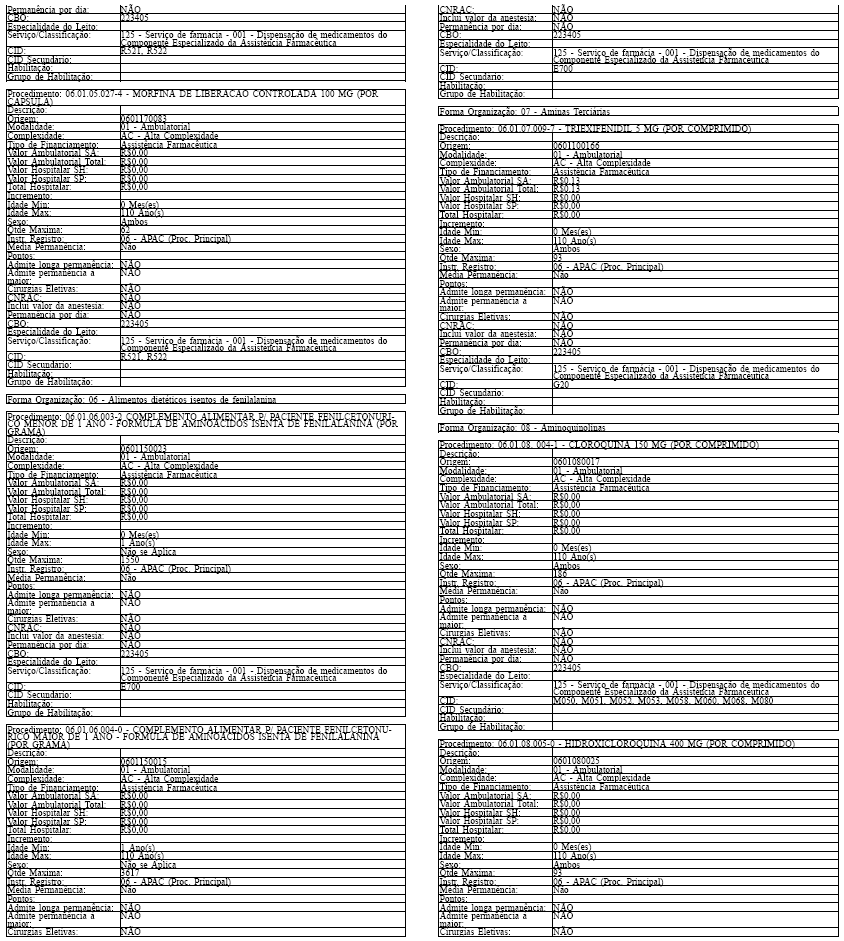
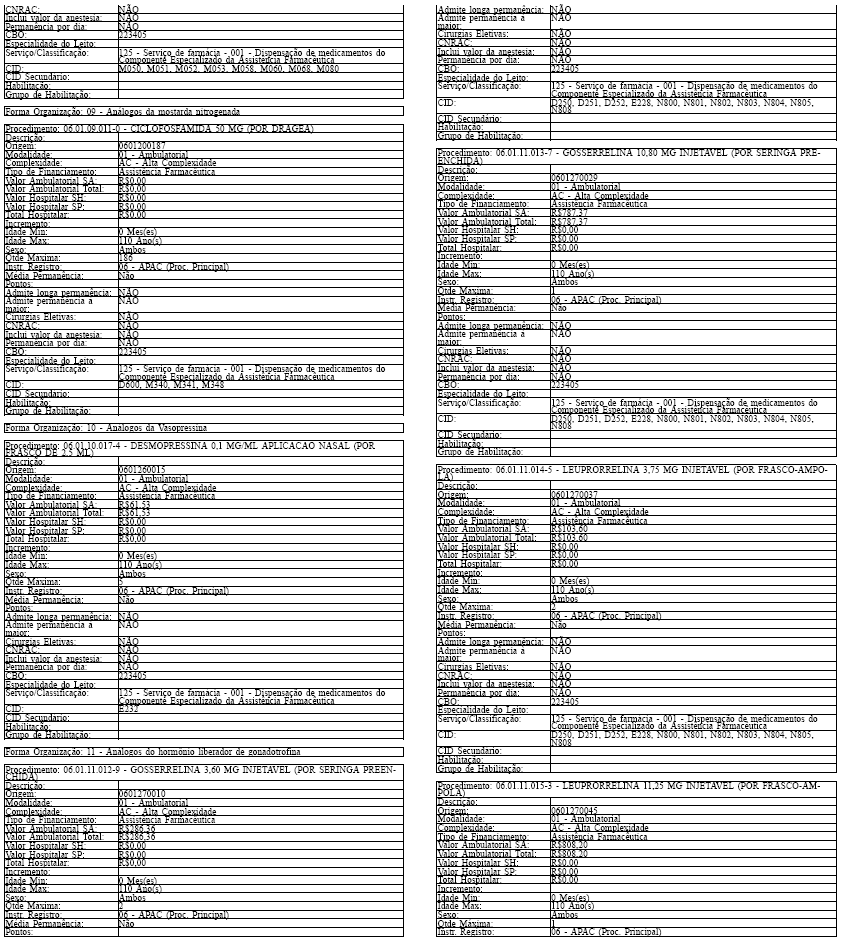
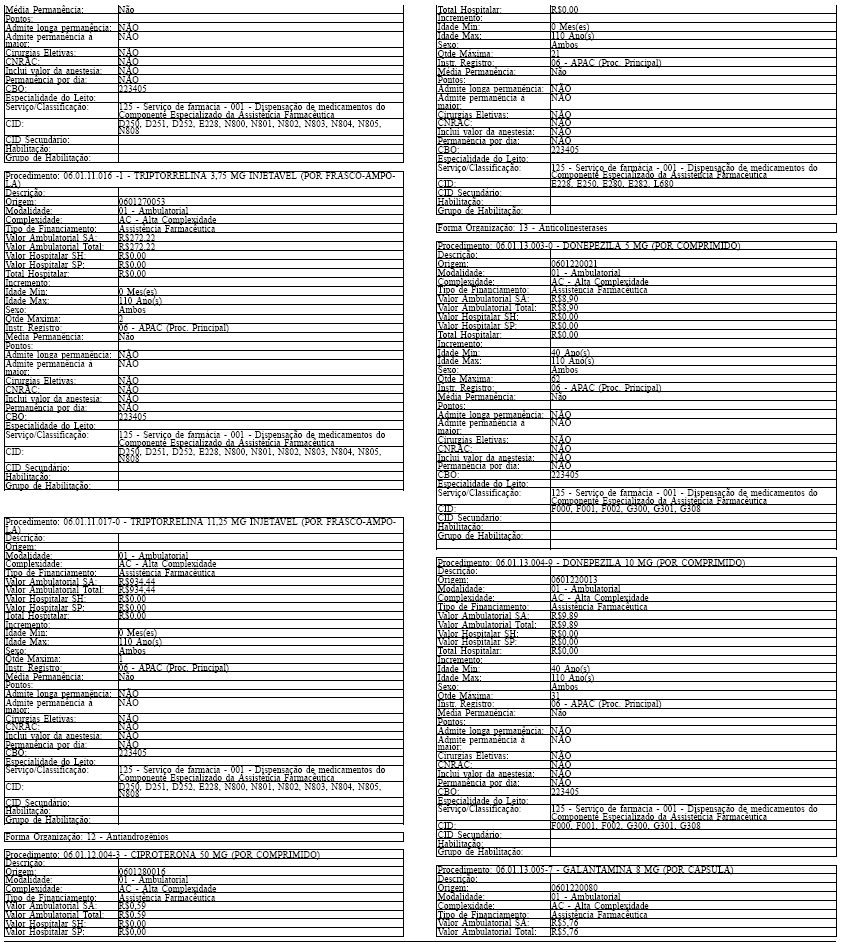
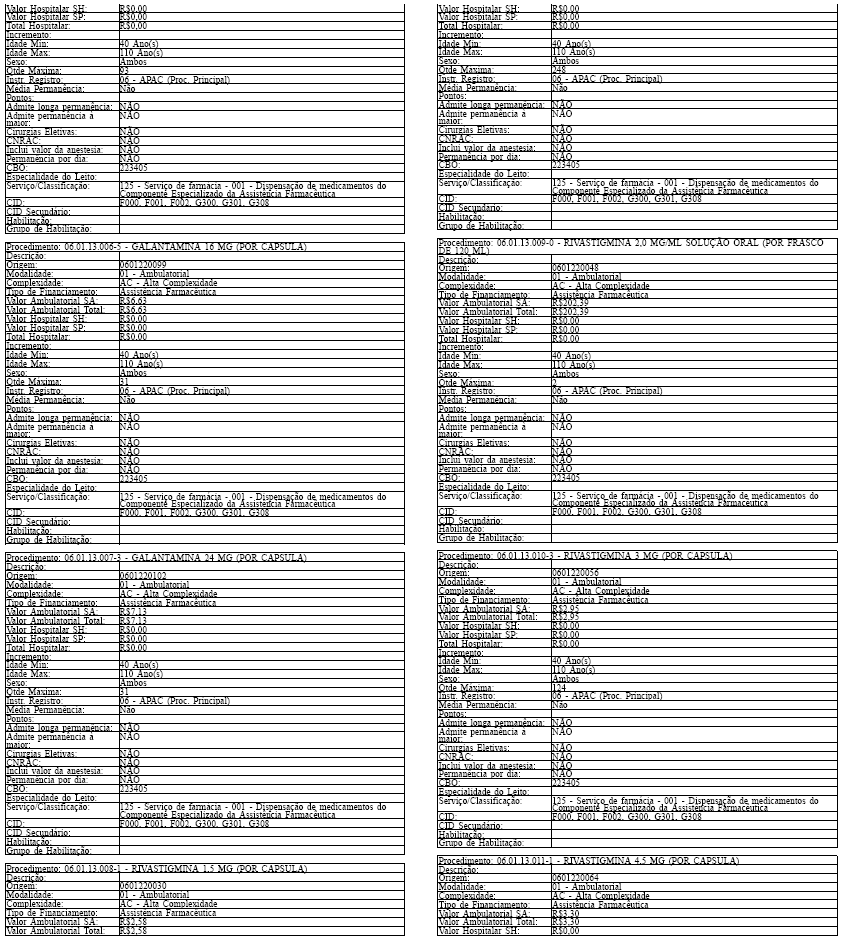
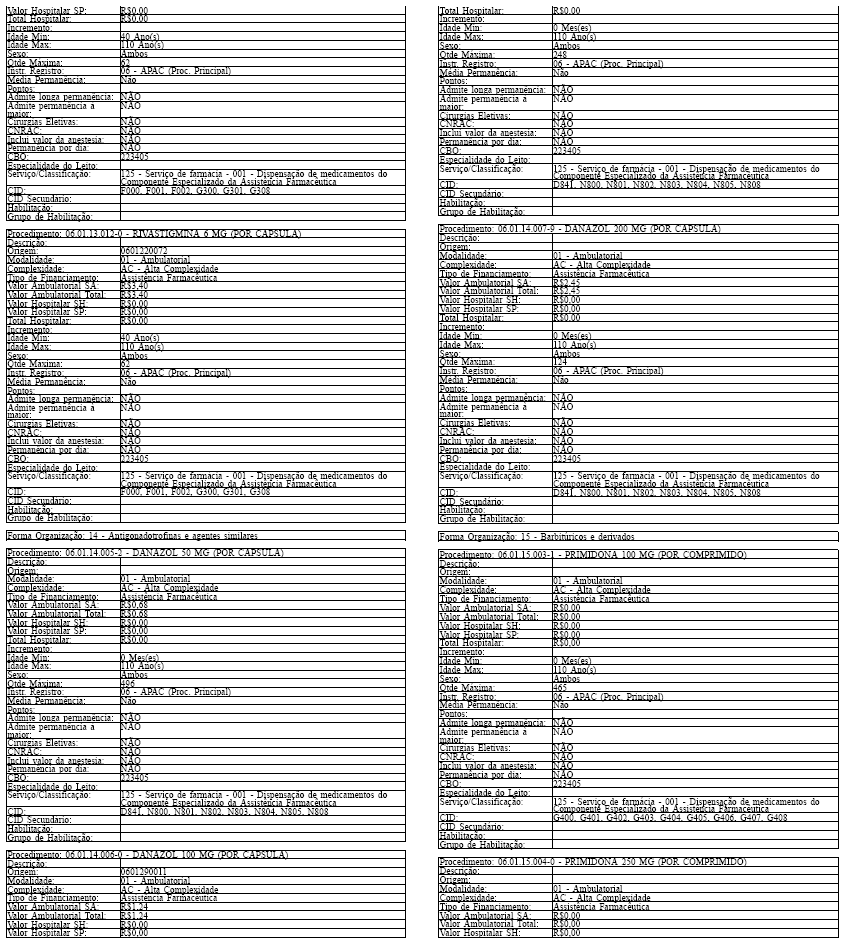

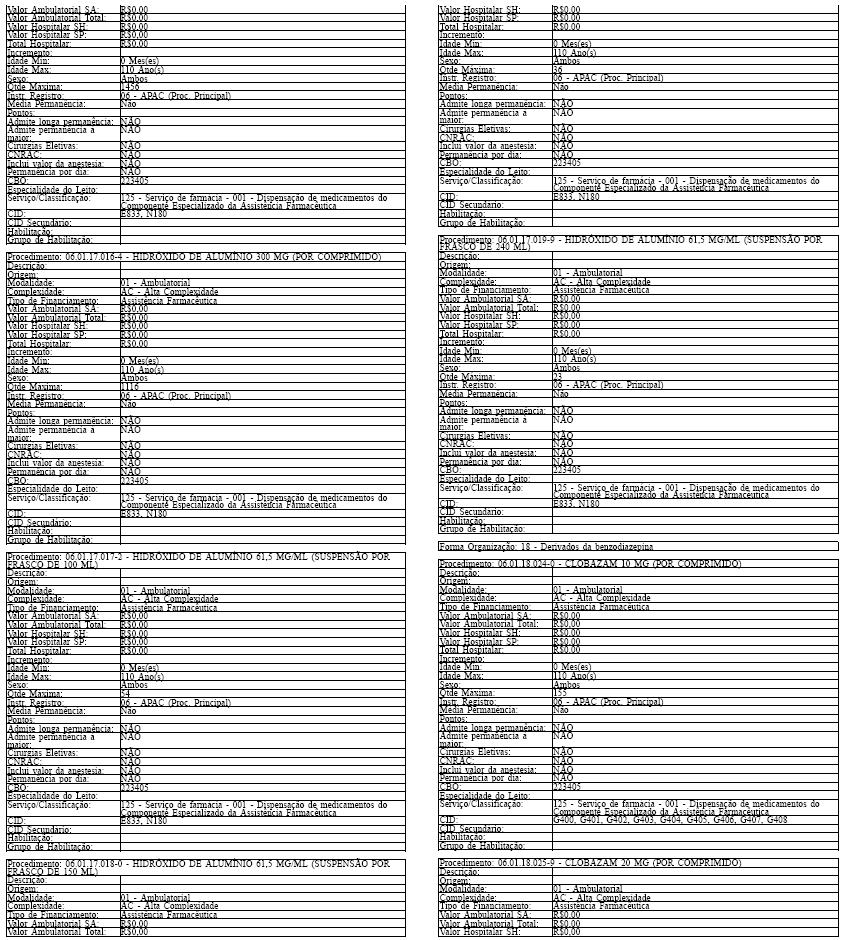

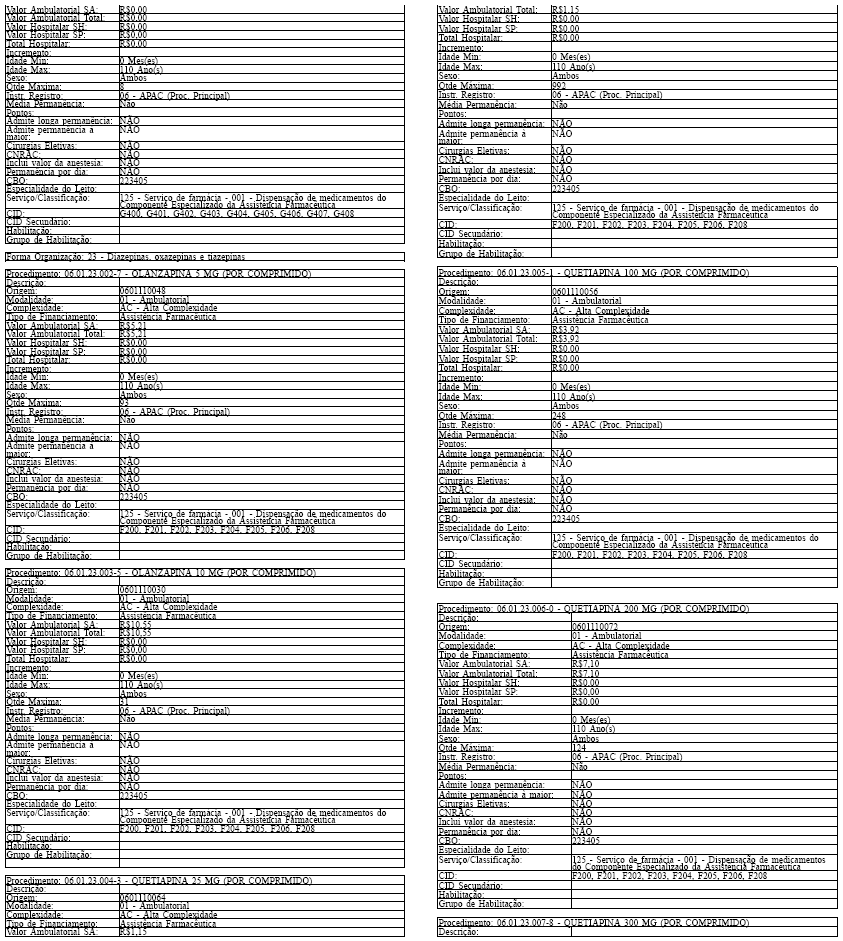
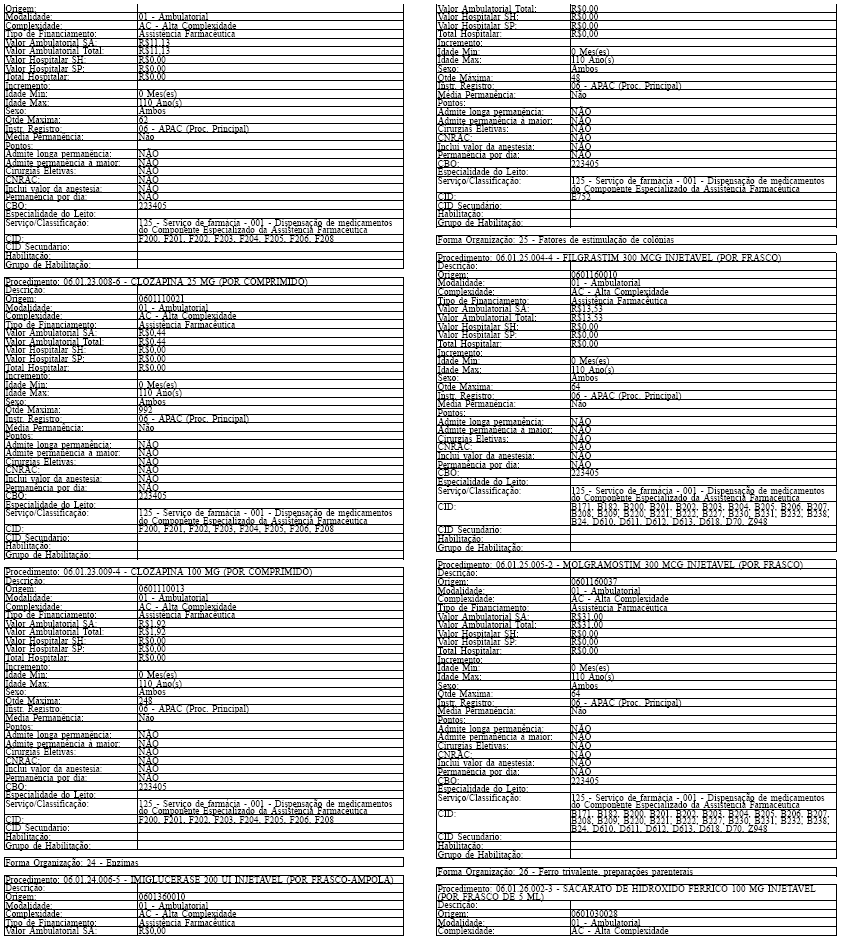
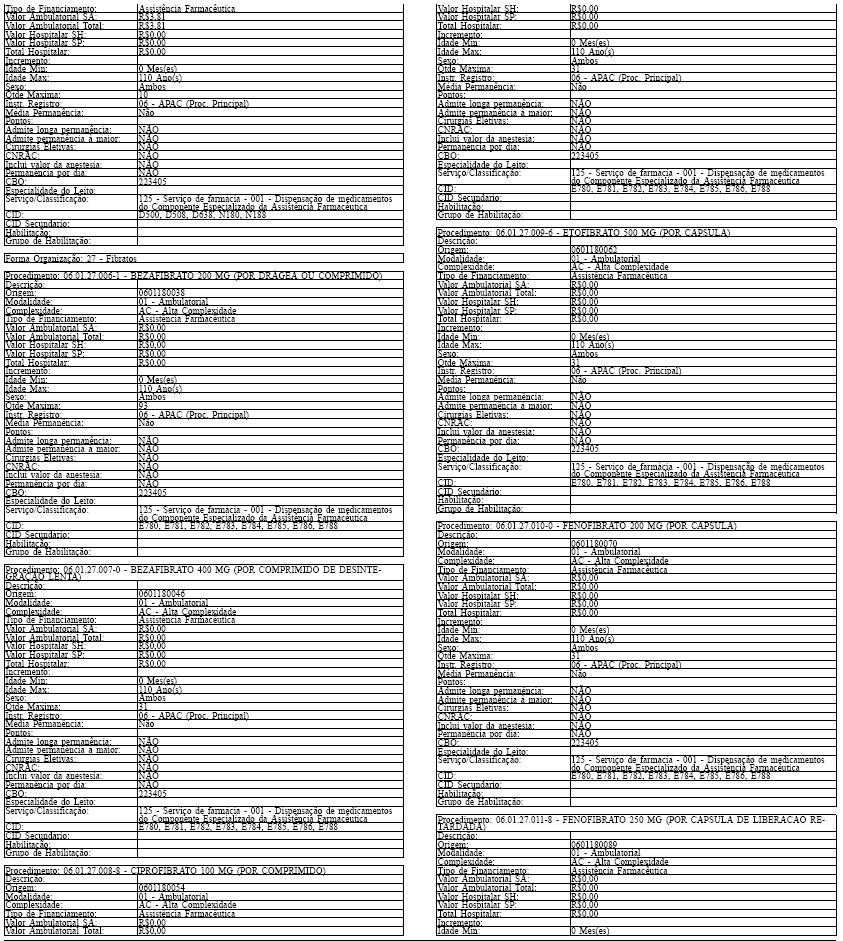
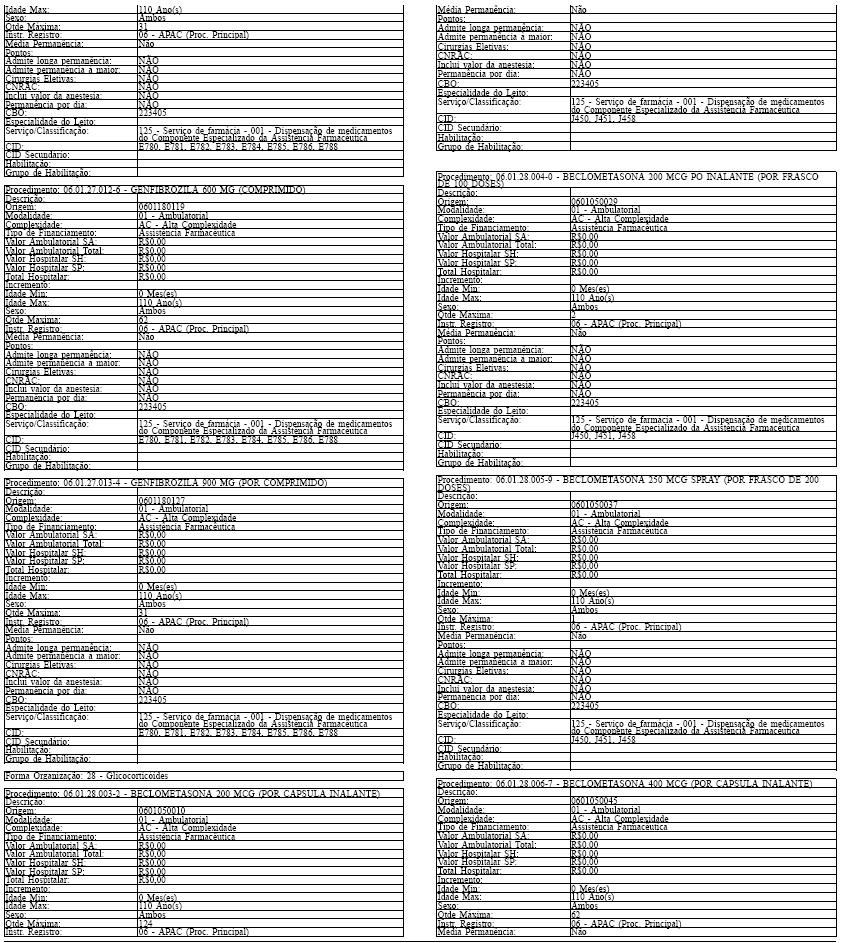
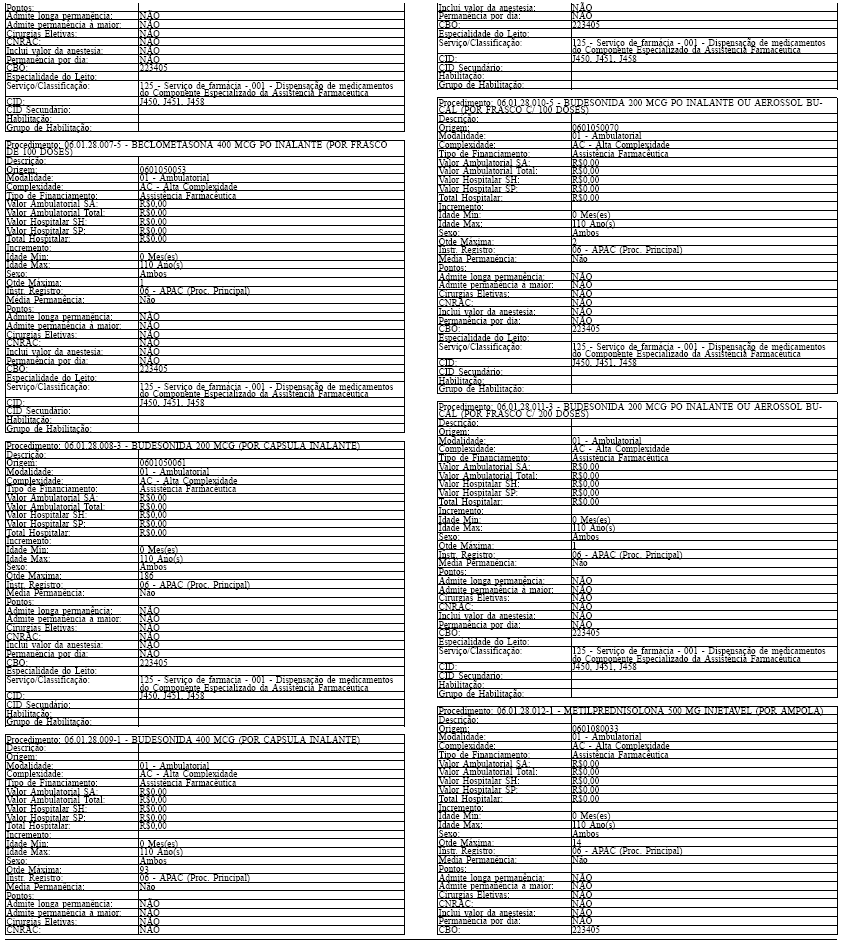
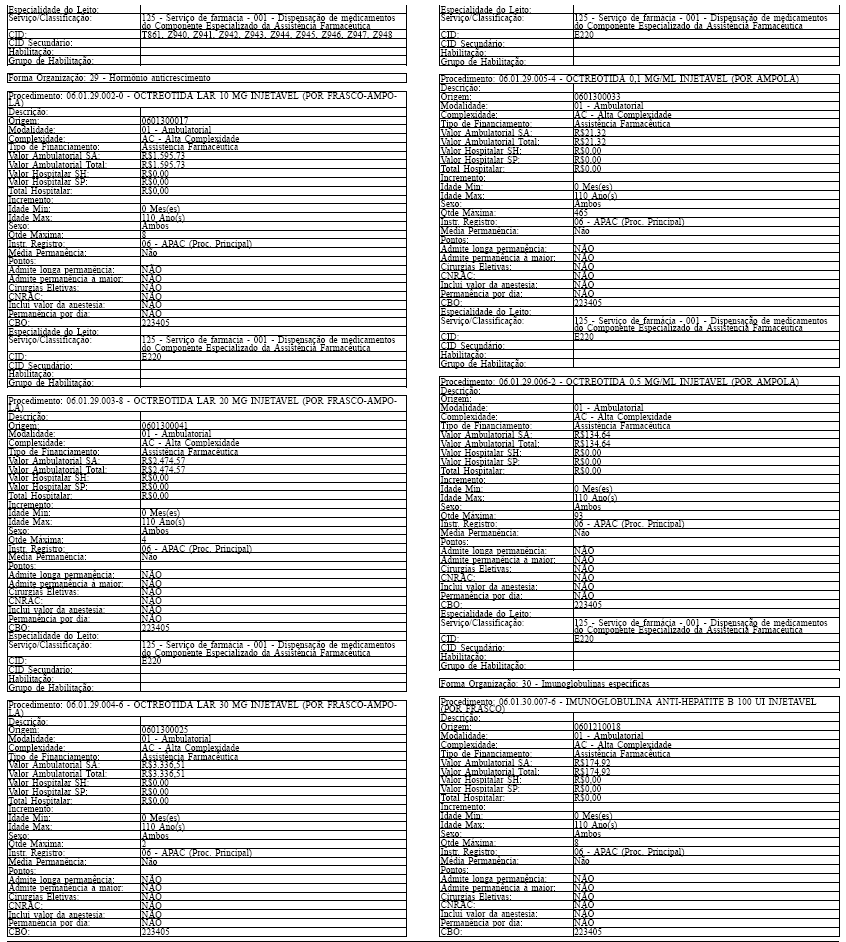


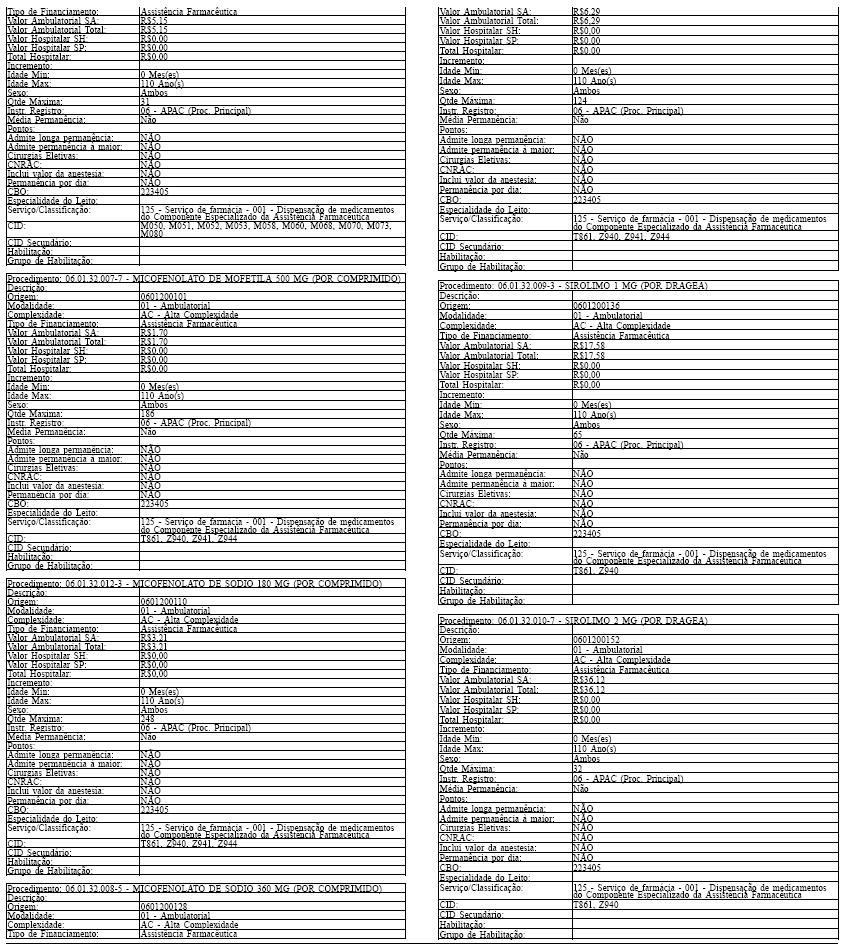
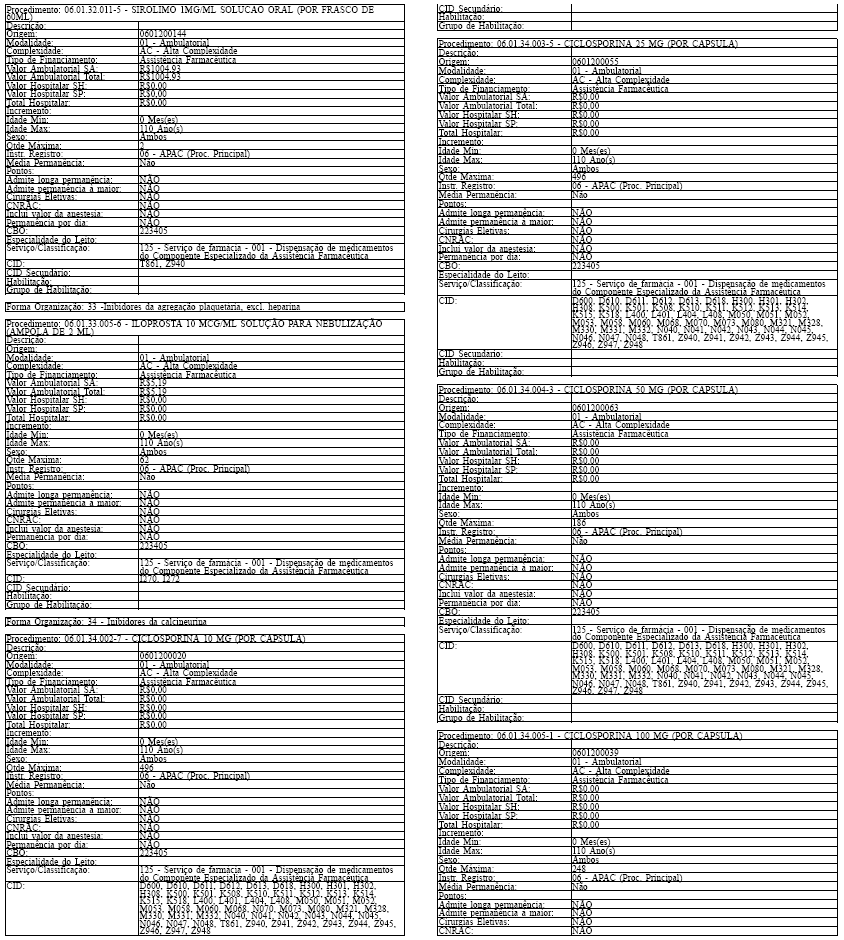
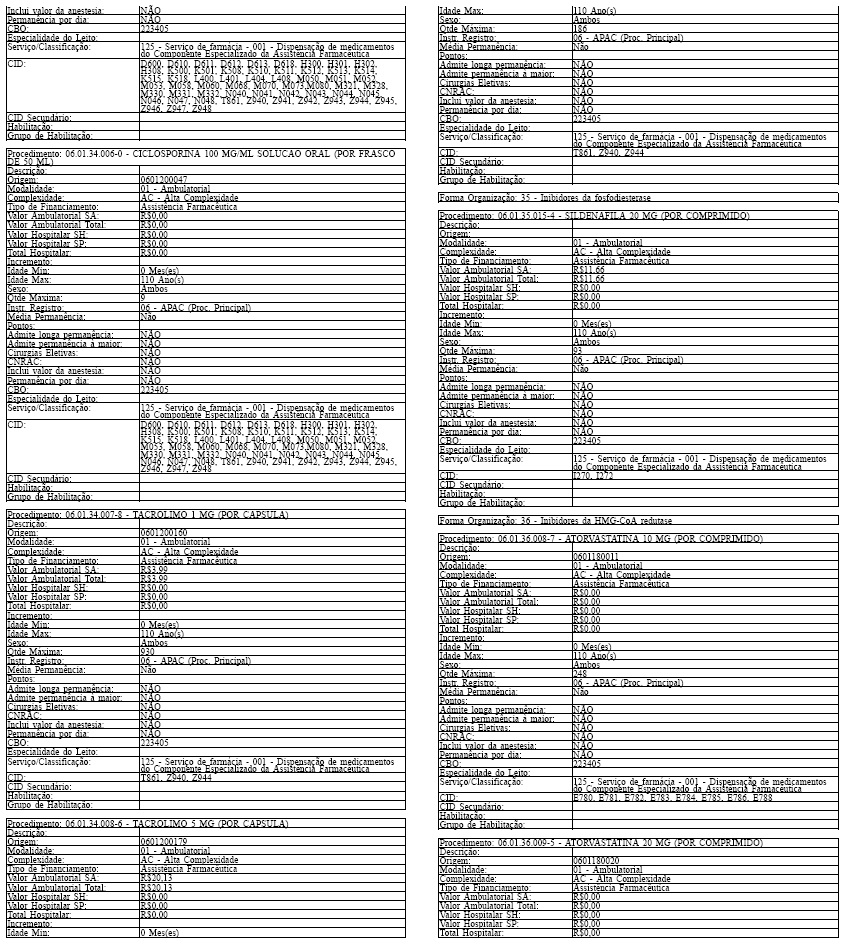
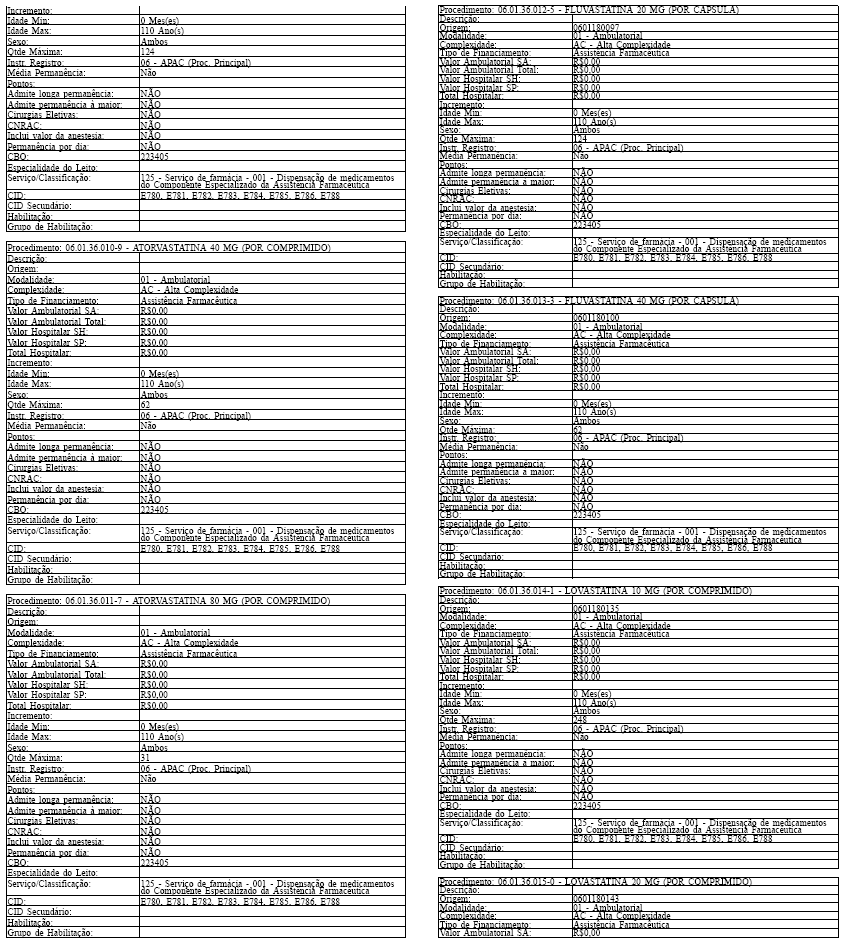
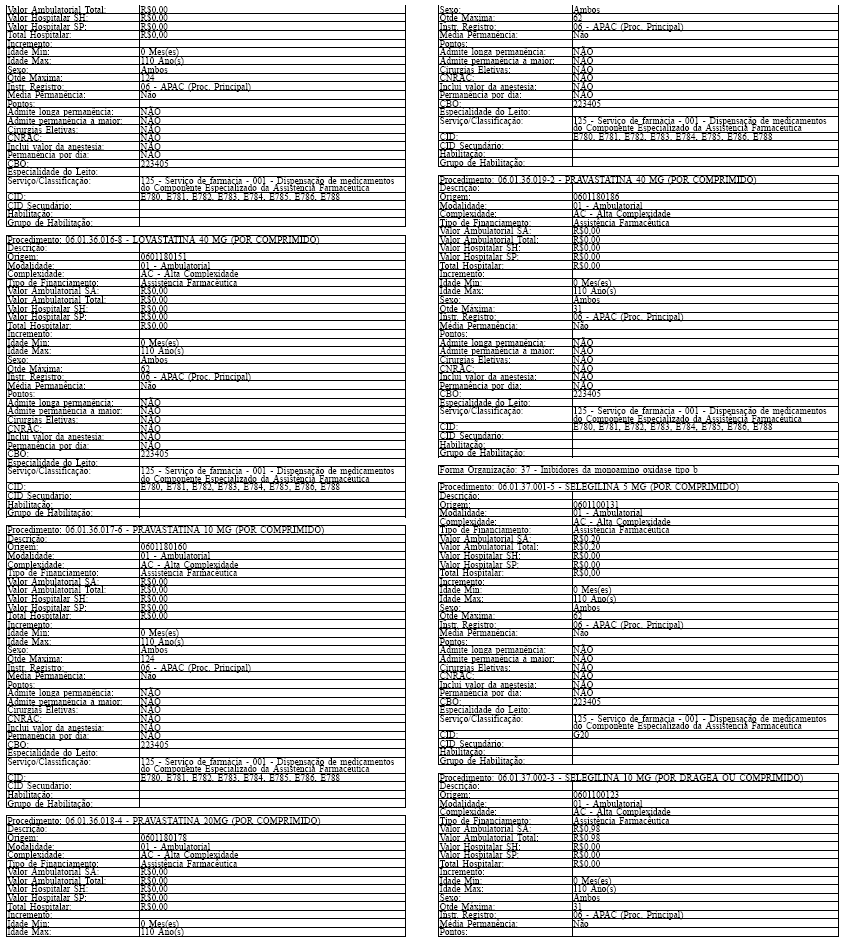
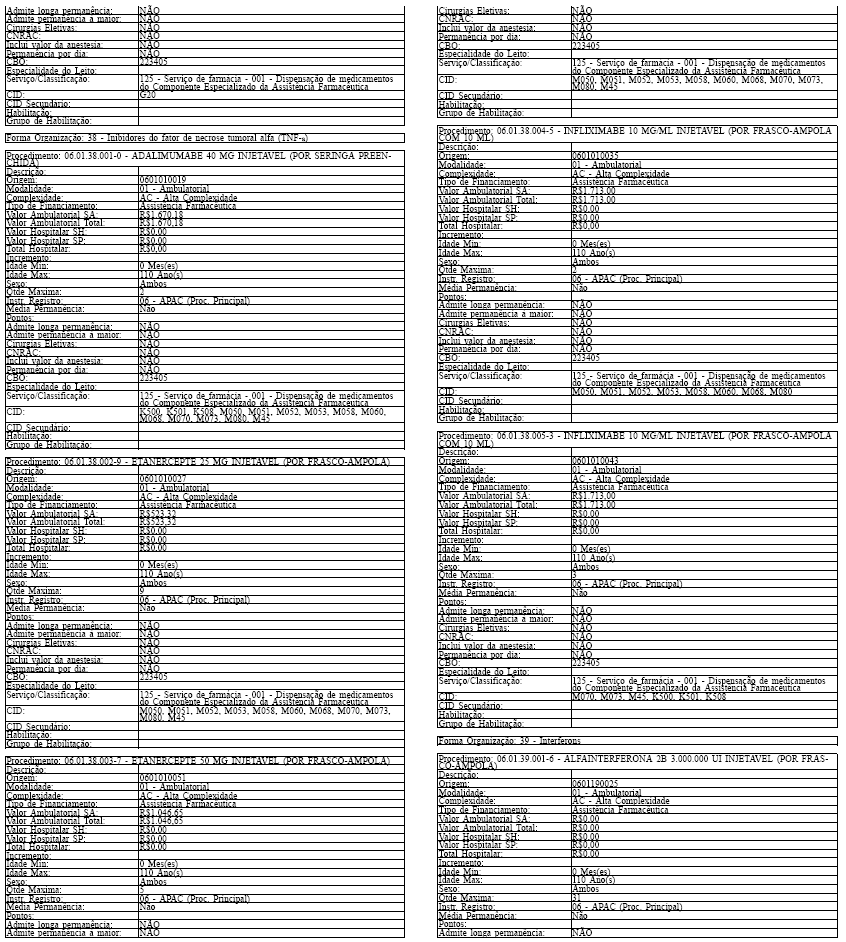
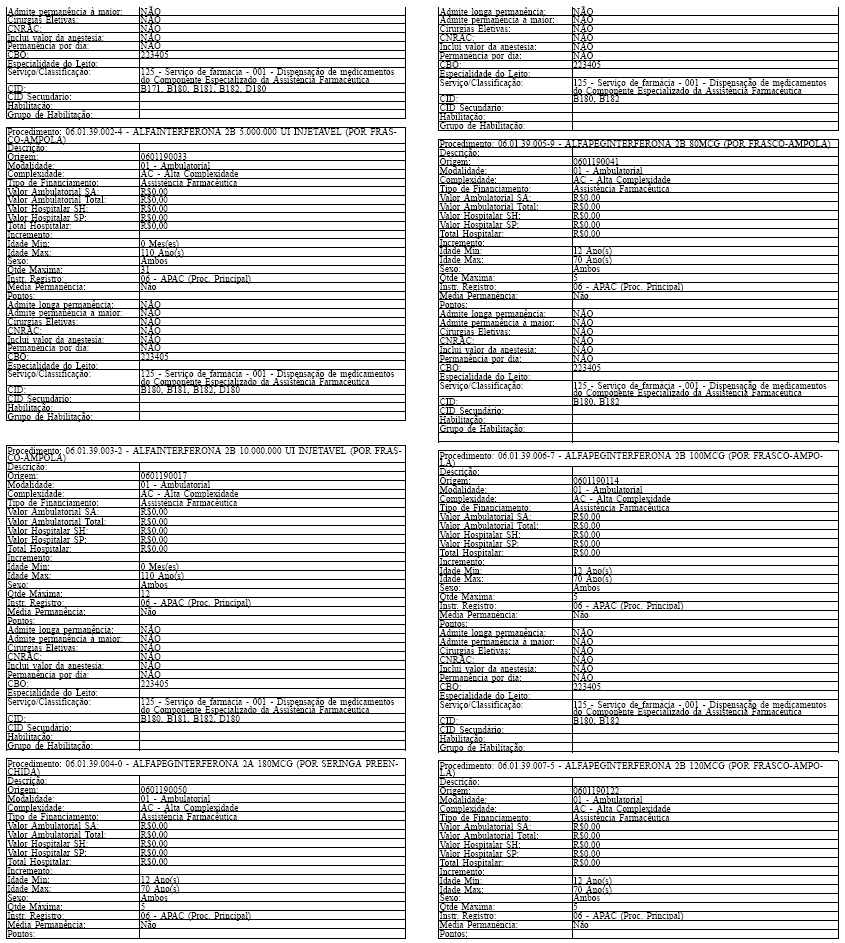
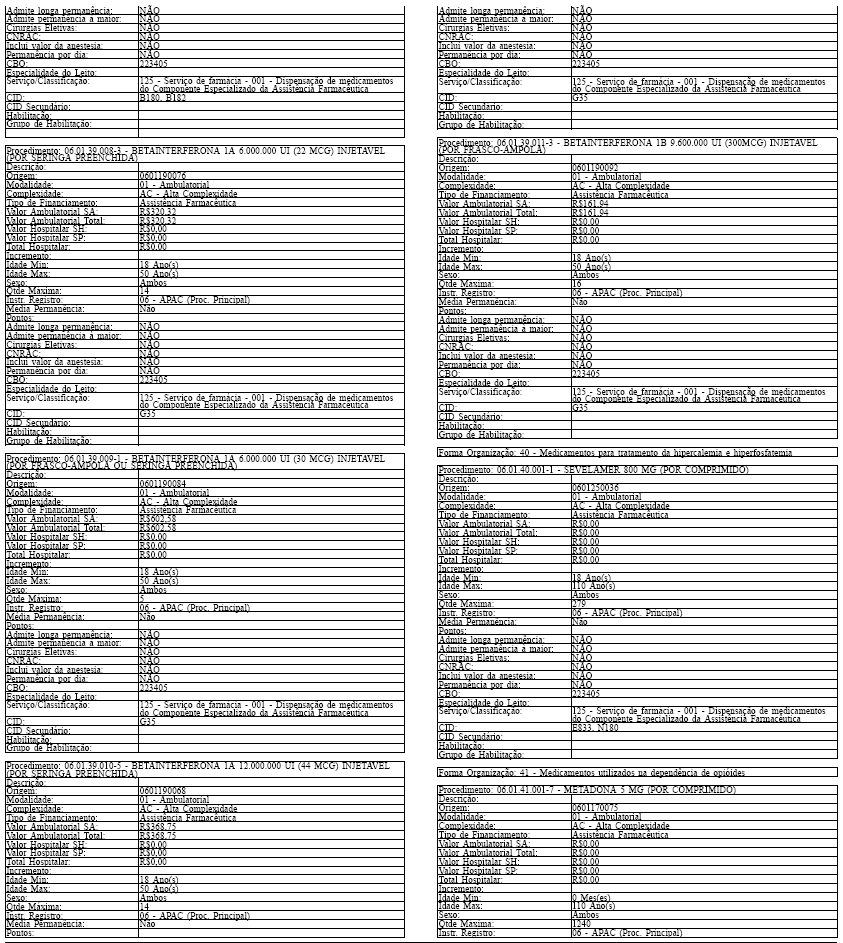
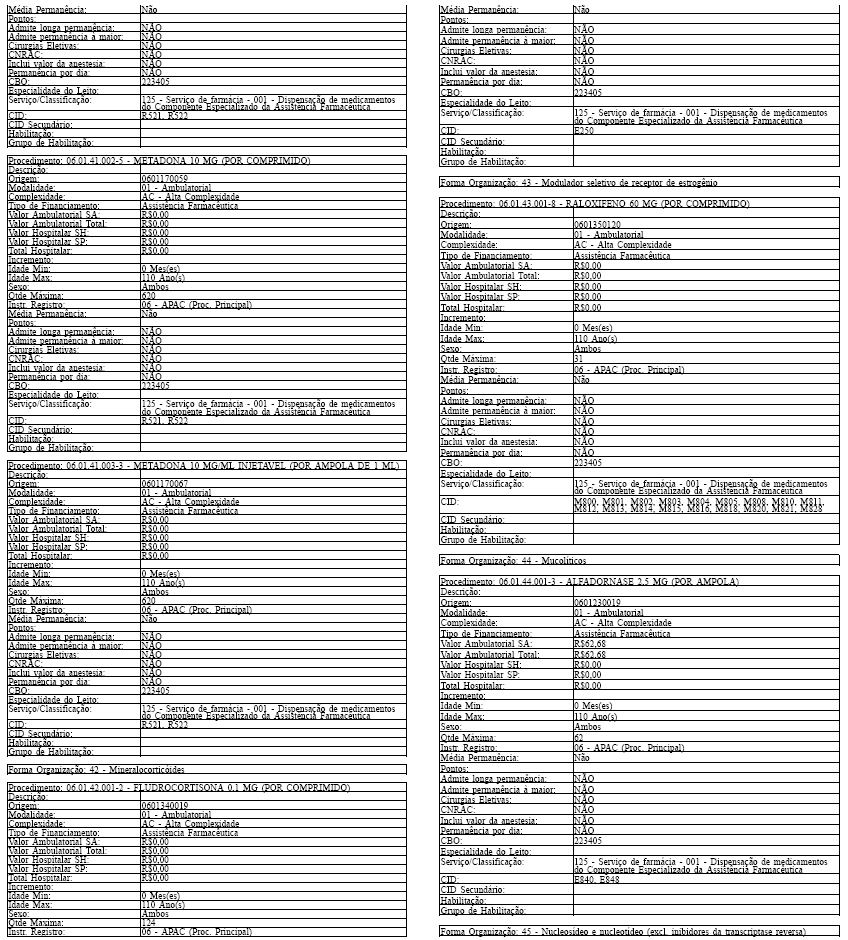
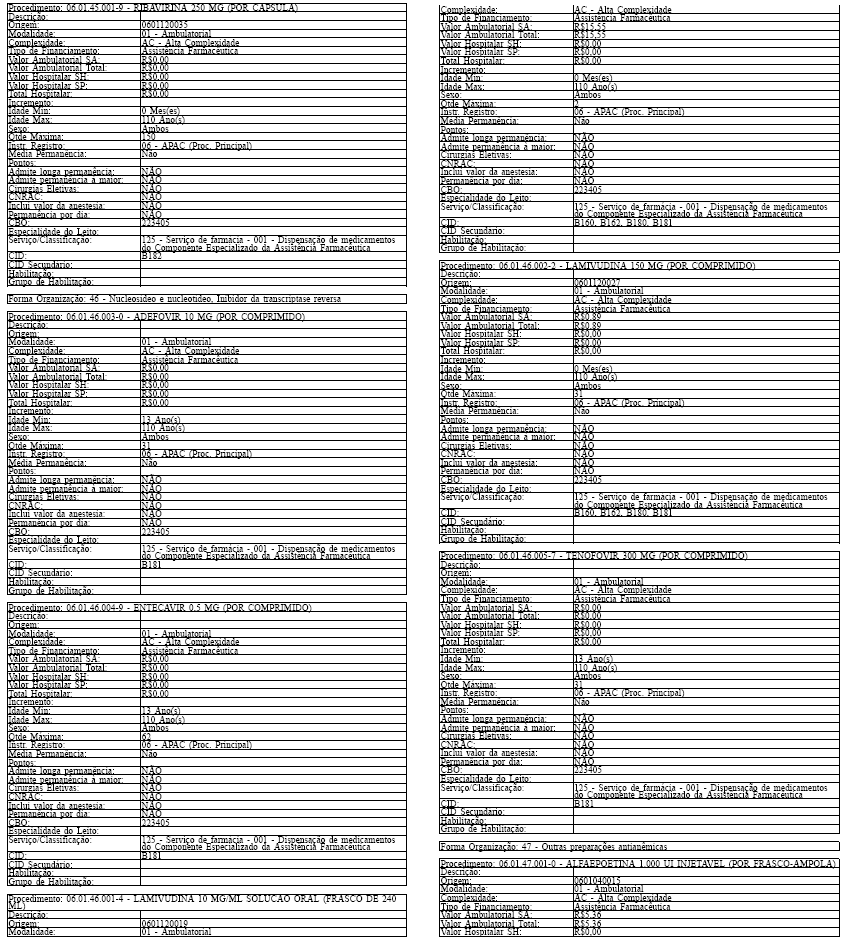

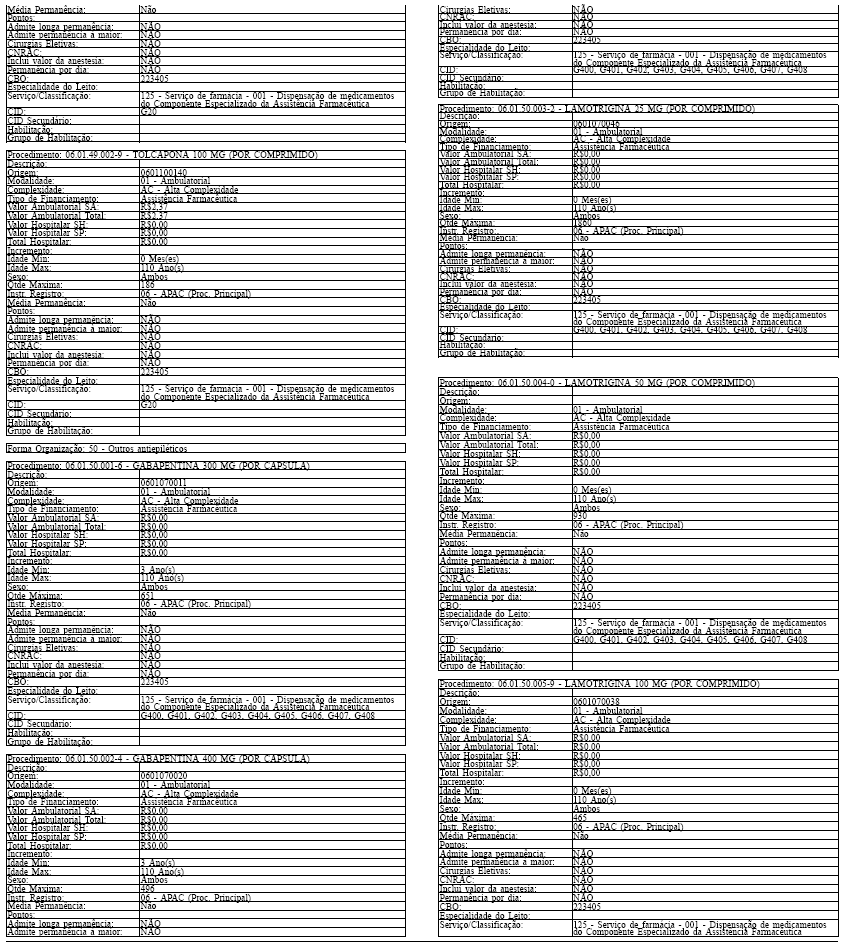
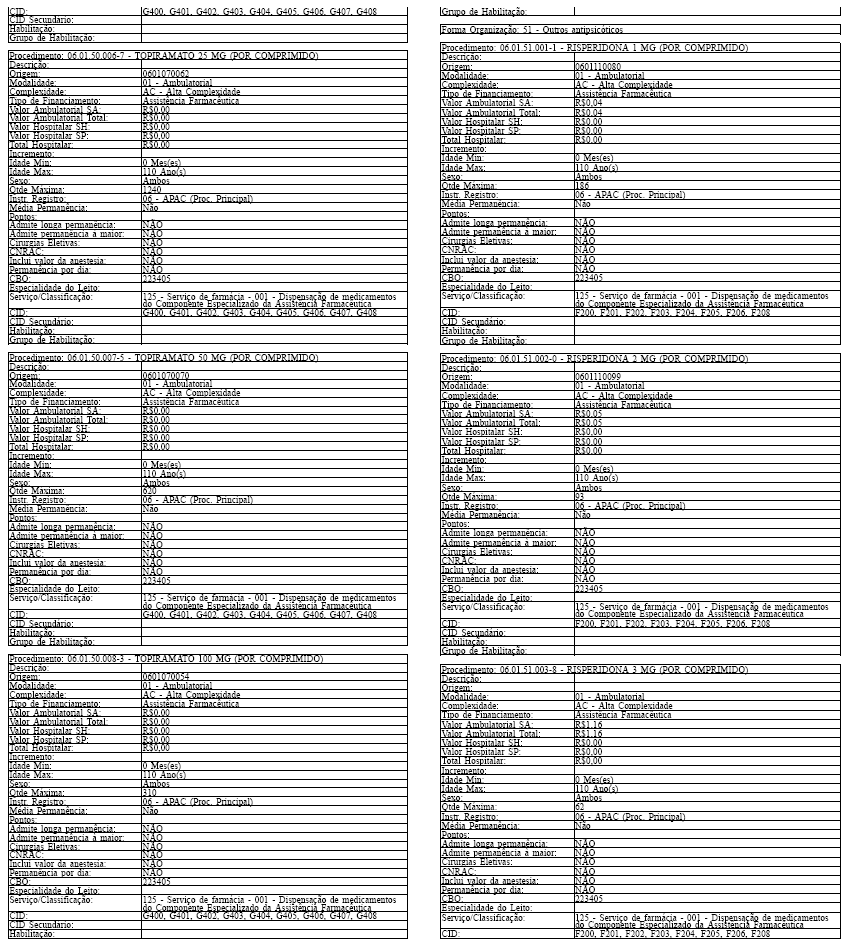

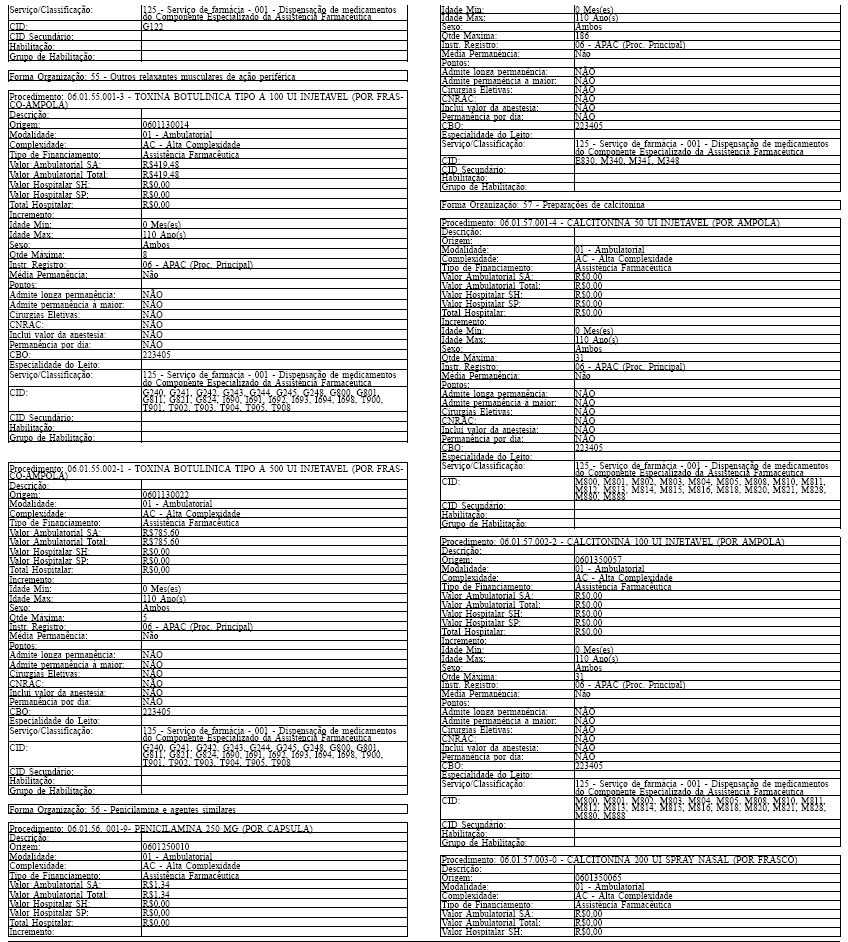
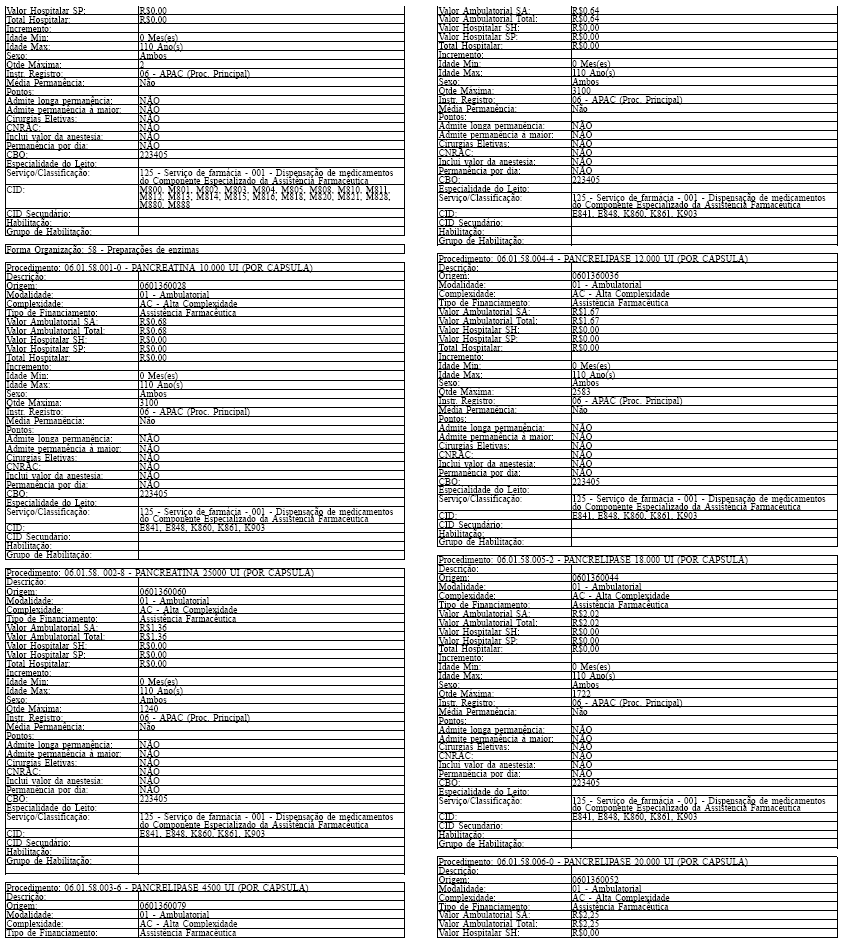
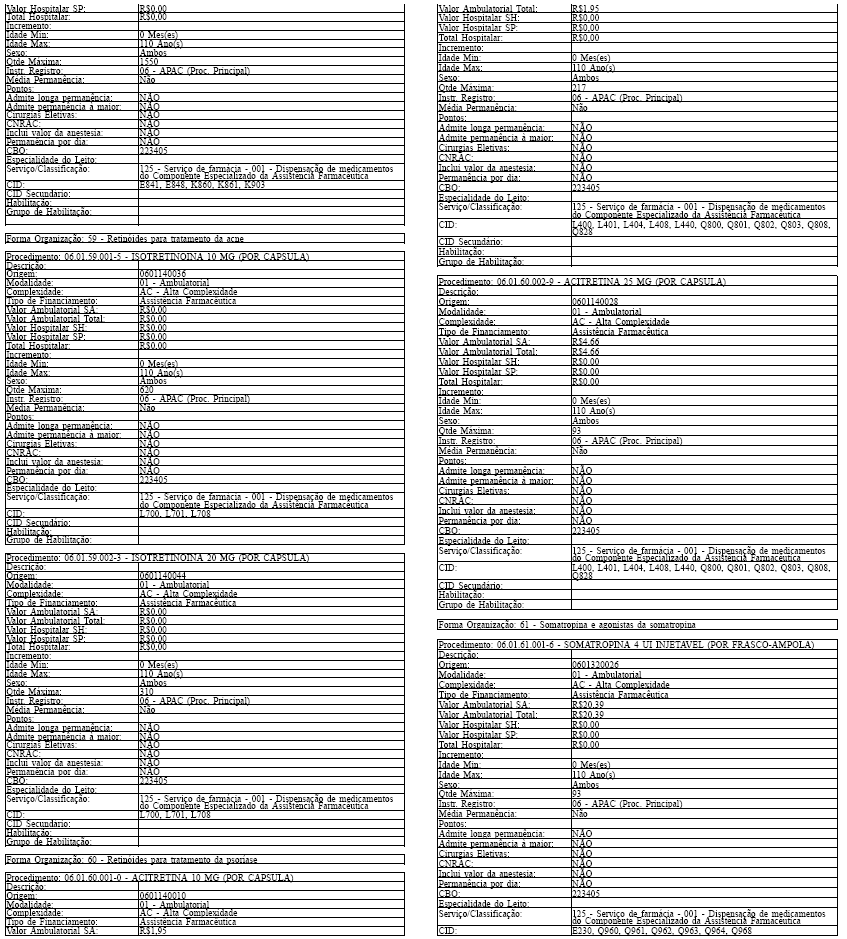
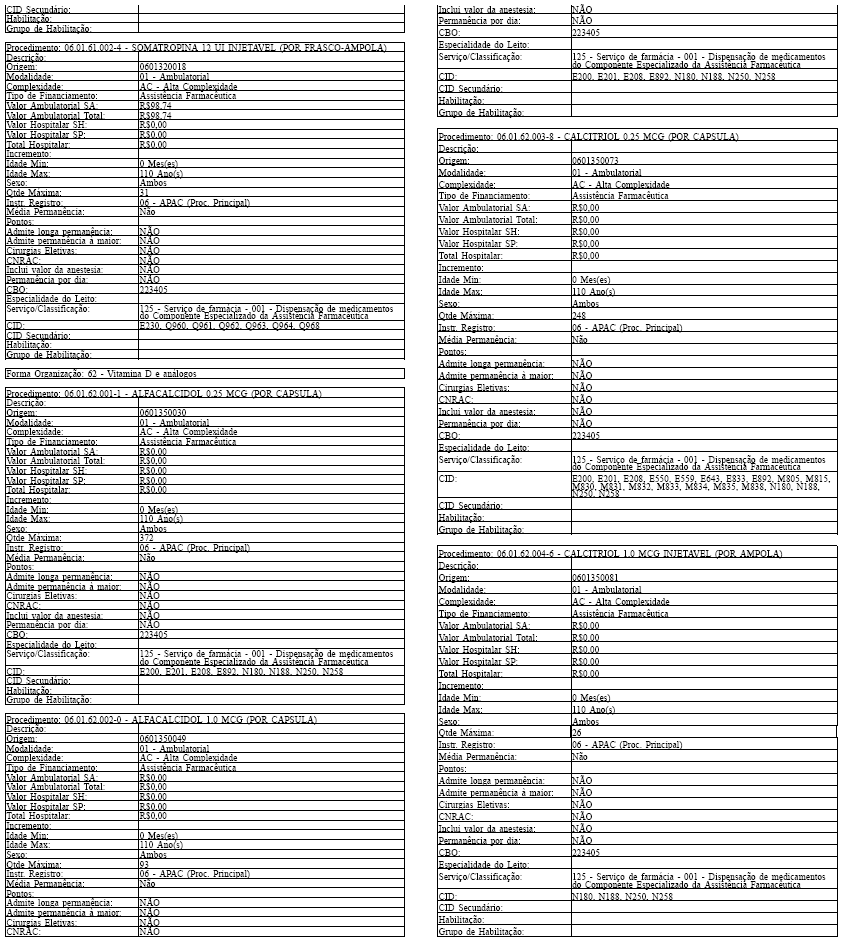
ANEXO V


LAUDO PARA SOLICITAÇÃO, AVALIAÇÃO E AUTORIZAÇÃO
DE MEDICAMENTOS DO COMPONENTE
ESPECIALIZADO
DA ASSISTÊNCIA FARMACÊUTICA
INSTRUÇÕES DE PREENCHIMENTO
SOLICITAÇÃO DO MEDICAMENTO
Campo 1 - Nome do Paciente: preencher com o nome completo do paciente sem abreviaturas.
Campo 2 - Cartão Nacional de Saúde (CNS): preencher com
o número do CNS do paciente.
Campo 3 - Nome do estabelecimento do médico solicitante:
preencher com o nome fantasia do estabelecimento de saúde ao qual
o médico solicitante está vinculado e que originou a solicitação de
medicamento(s).
Campo 4 - Cadastro Nacional de Estabelecimentos de Saúde (CNES): preencher com o código identificador do estabelecimento de saúde ao qual o médico solicitante está vinculado e que originou a solicitação de medicamento(s).
Campo 5 - Medicamento: preencher com o(s) nome(s) do(s) medicamentos(s) solicitado(s), de acordo com o descrito na Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde.
Campo 6 - Quantidade solicitada: preencher com a quantidade do(s) medicamento(s) solicitado(s) para cada mês de tratamento.
Campo 7 - Diagnóstico: diagnóstico da doença que motivou a solicitação do(s) medicamento(s), descrito com base na denominação da Classificação Estatística Internacional de Doenças e Problemas Relacionados à Saúde (CID-10).
Campo 8 - CID-10 Principal: preencher com o CID - 10 que corresponde à doença/lesão de base que motivou a solicitação do(s) medicamento(s).
Campo 9 - CID-10 Secundário: preencher com o CID -10 que corresponde à doença/lesão que iniciou a cadeia de acontecimentos patológicos que conduziram diretamente a doença de base. Campo de preenchimento não obrigatório.
Campo 10 - Anamnese: histórico do paciente que vai desde os sintomas iniciais até o momento da observação clínica, realizado com base nas lembranças do paciente.
Campo 11 - Alterações laboratoriais significativas: preencher, somente se necessário, as principais alterações laboratoriais que auxiliaram/definiram a doença em questão. Campo de preenchimento não obrigatório.
Campo 12 - Tratamentos prévios: preencher com os tratamentos medicamentoso(s) e/ou não medicamentoso(s) previamente utilizados pelo paciente para a doença em questão. Campo de preenchimento não obrigatório.
Campo 13 - Condição clínica do paciente: a solicitação do medicamento deverá ser realizada pelo paciente. Entretanto, fica dispensada a obrigatoriedade da presença daquele considerado incapaz de acordo com os artigos 3º e 4º do Código Civil: os menores de dezoito anos; aqueles que, por enfermidade ou deficiência mental, não tiverem o necessário discernimento para a prática desses atos ou que não puderem exprimir sua vontade, mesmo que transitória; ébrios habituais, viciados em tóxicos, ou os que, por deficiência mental, tenham o discernimento reduzido; os excepcionais, sem desenvolvimento mental completo; os pródigos. De acordo com a avaliação clínica pelo médico, descrever se o paciente preenche os critérios, ou não, de incapacidade. Caso apresente, descrever o nome completo do responsável pelo paciente.
Campo 14 - Nome do médico solicitante: preencher com o nome do profissional que solicita o procedimento, que deve estar cadastrado no CNES do estabelecimento solicitante.
Campo 15 - Data da solicitação: preencher com a data da solicitação, registrando o dia mês e ano no formato dd/mm/aaaa.
Campo 16 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo profissional solicitante no campo 17.
Campo 17 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo profissional solicitante.
Campo 18 - Assinatura e carimbo do médico: assinatura e carimbo com número de registro no Conselho de Classe do médico solicitante.
Campo 19 - Data de nascimento: preencher com a data de nascimento do paciente no formato dd/mm/aaaa.
Campo 20 - Altura: preencher com a altura do paciente, em metros, no dia do preenchimento.
Campo 21 - Peso: preencher com o peso do paciente, em quilogramas, no dia do preenchimento.
Campo 22 - Sexo: preencher com o sexo do paciente, assinalando com um "x" no quadro indicativo: M - Masculino ou F - Feminino.
Campo 23 - Município de residência/UF: preencher com o nome do município de residência do paciente e a sigla da unidade federativa a que pertence o município. Deve-se considerar como município de residência, o local fixo do paciente e não o de permanência temporária.
Campo 24 - Endereço: preencher com o endereço completo rua, número, complemento e bairro.
Campo 25 - Telefone de contato: preencher com número de telefone para possíveis contatos com o paciente.
Campo 26 - Nome da mãe ou responsável: preencher com o nome completo da mãe ou do responsável pelo paciente.
Campo 27 - Nome do profissional responsável pelo preenchimento: preencher com o nome do profissional que preencheu os dados complementares do paciente em questão, o qual deve estar cadastrado no CNES do estabelecimento solicitante.
Campo 28 - Data do preenchimento: preencher com a data do preenchimento dos dados complementares no formato dd/mm/aaaa.
Campo 29 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo profissional responsável pelo preenchimento dos dados complementares do paciente no campo 30.
Campo 30 - Nº documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo profissional responsável pelo preenchimento dos dados complementares do paciente.
Campo 31 - Assinatura do responsável pelo preenchimento: assinatura do profissional responsável pelo preenchimento dos dados complementares do paciente.
AVALIAÇÃO TÉCNICA
Campo 1 - Nome do paciente: preencher com o nome completo do paciente sem abreviaturas.
Campo 2 - Cartão Nacional de Saúde (CNS): preencher com o número do CNS do paciente.
Campo 3 - Código(s)/ Medicamento(s): preencher com os medicamentos solicitados e seus respectivos códigos da Tabela de Procedimentos, Medicamentos, Órteses, Próteses e Materiais Especiais do Sistema Único de Saúde, de preferência, na mesma ordem da solicitação.
Campo 4 - CID-10 principal: preencher com o CID-10 principal descrito pelo médico solicitante.
Campo 5 - CID-10 secundário: preencher com o CID-10 secundário descrito pelo médico solicitante. Caso o médico não o descreveu, deixar este campo em branco.
Campo 6 - Deferimento: o deferimento deve ocorrer quando a solicitação de algum medicamento preenche os critérios descritos no Protocolo Clínico e Diretrizes Terapêuticas da referida doença, publicado pelo Ministério da Saúde, na versão final, e os demais parâmetros definidos do Componente Especializado da Assistência Farmacêutica. Assinalar o(s) números(s) correspondentes ao(s) medicamento(s) deferido(s).
Campo 7 - Devolução: a devolução caracteriza-se pela ausência de informação ou de documentos/exames ou preenchimento incorreto da solicitação do medicamento que impedem a plenitude da análise. Deve-se assinalar qual o motivo da devolução e o(s) número(s) correspondente(s) ao(s) medicamento(s) devolvido(s), considerando as seguintes definições: Preenchimento incompleto: assinalar quando há falta de preenchimento de algum campo considerado obrigatório no campo de solicitação de medicamento(s); Preenchimento incorreto: assinalar quando em algum campo da solicitação de medicamento(s) foi descrita informação incorreta da descrita nesta Instrução; Ausência de documentação: assinalar no caso de ausência de alguma documentação exigida pelo Protocolo Clínico e Diretrizes Terapêuticas da doença em questão ou pelo Componente Especializado da Assistência Farmacêutica; Ausência de exame: assinalar no caso de ausência de algum exame exigido pelo Protocolo Clínico e Diretrizes Terapêuticas da doença em questão; Outros: assinalar quando o motivo de devolução não se enquadrar nos demais parâmetros descritos acima.
Campo 8 - Especificação: descrever, se necessário, informações complementares que auxiliem no esclarecimento do motivo da devolução.
Campo 9 - Indeferimento: o indeferimento caracteriza-se pela negativa da solicitação do(s) medicamento(s), seja por não preencher os critérios estabelecidos pelo Protocolo Clínico e Diretrizes Terapêuticas da referida doença, publicado pelo Ministério da Saúde, na versão final, e/ou os demais parâmetros definidos no Componente Especializado da Assistência Farmacêutica. Deve-se assinalar qual o motivo da devolução e o(s) número(s) correspondente(s) ao(s) medicamento(s) devolvido(s), quando necessário, considerando as seguintes definições: Não preenche critérios do Protocolo Clínico e Diretrizes Terapêuticas: assinalar quando a solicitação de medicamento(s) não preenche os critérios estabelecidos no Protocolo Clínico e Diretrizes Terapêuticas, devido a condição clínica/laboratorial do paciente ou por não possuir indicação do(s) referido(s) medicamento(s), no momento da solicitação; Medicamento não padronizado: assinalar quando há solicitação de medicamento(s) não padronizado no Componente Especializado da Assistência Farmacêutica; CID-10 não padronizado: assinalar no caso que o CID-10 Primário, descrito pelo médico solicitante, não está padronizado no Componente Especializado da Assistência Farmacêutica; Outros: assinalar quando o motivo de indeferimento não se enquadrar nos demais parâmetros descritos acima.
Campo 10 - Especificação: descrever, se necessário, informações complementares que auxiliem a esclarecer o motivo do indeferimento.
Campo 11 - Nome do avaliador: preencher com o nome completo do avaliador.
Campo 12 - Data da avaliação: preencher com a data da avaliação no formato dd/mm/aaaa.
Campo 13 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo avaliador no campo 14.
Campo 14 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo avaliador.
Campo 15 - Assinatura e Carimbo do avaliador: assinatura e carimbo do avaliador.
AUTORIZAÇÃO
Campo 1 - Autorização: assinalar se a solicitação de um ou mais medicamentos, previamente deferidos pelo avaliador, poderá ser autorizada. Assinalar o(s) números(s) correspondentes ao(s) medicamento(s) autorizado(s).
Campo 2 - Especificação: descrever, se necessário, informações complementares que auxiliem a esclarecer o motivo da não autorização ou demais parâmetros que justificam alguma alteração.
Campo 3 - Número da Autorização de Procedimento de Alto Custo (APAC): Descrever o número de APAC (Autorizações de Procedimento de Alta Complexidade/Custo no Sistema de Informações Ambulatoriais do SUS - SIA/SUS) gerado.
Campo 4 - Vigência: Descrever o período de vigência da APAC .
Campo 5 - Nome do autorizador: preencher com o nome do autorizador.
Campo 6 - Data da autorização: preencher com a data da autorização, registrando o dia, mês e ano no formato dd/mm/aaaa.
Campo 7 - Documento: assinalar com um "x" no campo correspondente ao CNS ou CPF que será descrito pelo autorizador no campo 08.
Campo 8 - Nº Documento: preencher com o nº do documento (CNS ou CPF) utilizado pelo autorizador
Campo 9 - Assinatura e carimbo do autorizador: assinatura e carimbo do autorizador
ANEXO VI

(*) Republicada por ter saído, no DOU nº 228, de 30-11-2009, Seção 1, págs. 725 a 771, com erro de montagem.